题目内容
4.B氮元素可以形成多种化合物.回答以下问题:
(1)基态氮原子的价电子排布式是2s22p3.
(2)C、N、O三种元素第一电离能从大到小的顺序是N>O>C.
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被--NH2(氨基)取代形成的另一种氮的氢化物.
①NH3分子的空间构型是三角锥形;N2H4分子中氮原子轨道的杂化类型是sp3.
②肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)△H=-1 038.7kJ•mol-1若该反应中有4mol N-H键断裂,则形成的π键有3mol.
③肼能与硫酸反应生成N2H6SO4,N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在d(填标号).
a.离子键 b.共价键c.配位键 d.范德华力
(4)NH3 与BF3可以通过配位键形成NH3.BF3分子,其中N原子提供孤电子对,B原子提供空轨道.
分析 (1)N原子核外有7个电子,最外层有5个电子,根据构造原理顺序其价电子排布式;
(2)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素;
(3)①根据价层电子对互斥理论确定分子空间构型和原子的杂化方式;
②反应中有4mol N-H键断裂,生成1.5molN2,根据结构式N≡N判断;
③根据硫酸铵晶体中存在的化学键判断;
(4)B原子含有3个σ 键一个配位键,B原子提供空轨道的原子、N原子提供孤电子对.
解答 解:(1)氮原子的电子排布式1s22s22p3,其价层电子排布式为2s22p3,故答案为:2s22p3;
(2)C、N、O属于同一周期元素且原子序数依次减小,同一周期元素的第一电离能随着原子序数的增大而增大,但第ⅤA族的大于第ⅥA族的,所以其第一电离能大小顺序是N>O>C,故答案为:N>O>C;
(3)①NH3分子中氮原子含有3个共价键和一个孤电子对,所以空间构型是三角锥型;N2H4分子中氮原子的价层电子对=3+1=4,含有一个孤电子对,N原子轨道的杂化类型是sp3,
故答案为:三角锥型;sp3;
②1mol氮气分子中含有2molπ键,若该反应中有4mol-H键断裂,即有1mol肼参加反应,生成1.5mol氮气,所以形成的π键有1.5mol×2=3mol,故答案为:3;
③3N2H6SO4和(NH4)2SO4都是离子晶体,N2H6 2+和SO42-之间存在离子键,N2H62+中N和H之间形成6个共价键(其中2个配位键),N和N之间形成共价键,SO42-中S和O之间形成共价键,不含范德华力,
故答案为:d;
(4)BF3•NH3中B原子其价层电子数是4,采取sp3杂化,B原子含有3个σ 键一个配位键,该化合物中,B原子提供空轨道的原子、N原子提供孤电子对,B、N原子之间形成配位键,
故答案为:N;B.
点评 本题考查了电子排布式、第一电离能的比较、原子的杂化方式的判断、化学键、等电子体等知识点,题目难度中等,注意分子空间构型的判断及原子杂化方式的判断是高考的热点.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案| A. | 向CuSO4溶液中加入NaOH溶液得到的分散系 | |
| B. | 向水中加入食盐得到的分散系 | |
| C. | 向沸水中滴入饱和FeCl3溶液得到的红褐色液体 | |
| D. | 向NaOH溶液中通入CO2得到的无色溶液 |
 )甲酯并计算其产率.实验步骤如下:
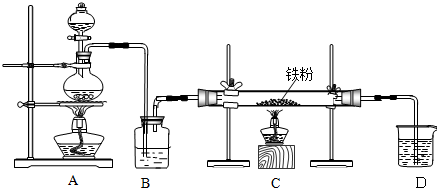
)甲酯并计算其产率.实验步骤如下:Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,以及约10mL甲苯(甲苯与
 水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯5.3g.
常用物理常数如下:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)实验中加入沸石的作用是防暴沸;
(3)加入甲苯的作用是将反应产生的水从反应体系中分离出来,使合成水杨酸甲酯反应的化学平衡向右移动,从而提高反应的产率.
(4)反应结束后,分离甲醇所采用操作的名称是蒸馏.
(5)洗涤操作中,前后两次水洗的目的分别是为了洗掉洗掉大部分硫酸和洗掉碳酸氢钠.
(6)在蒸馏操作中,仪器选择及安装都正确的是(填标号)b.

(7)本实验的产率为70%(保留两位有效数字).
| A. | 原子最外层电子数大于4的元素可能是金属元素 | |
| B. | 含有共价键的物质一定是共价化合物 | |
| C. | 离子化合物中只可能含有离子键而不可能含有共价键 | |
| D. | 多种非金属元素之间形成的共价键一定是极性键 |
| A. | 电子层序数越大,s原子轨道的形状相同、半径越大 | |
| B. | 在同一电子层上运动的电子,其自旋方向肯定不同 | |
| C. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| D. | 原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解 |
| A. | 0.1mol/L的醋酸溶液中c(H+)=0.1mol/L | |
| B. | 0.1mol/L 的NaClO溶液中pH>7 | |
| C. | 任何一个化学变化都伴随着能量的变化 | |
| D. | 新制的氯水中存在着三种分子 |
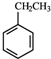 (g)+CO2(g)?
(g)+CO2(g)?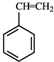 (g)+CO(g)+H2O(g)△H=-166KJ/mol
(g)+CO(g)+H2O(g)△H=-166KJ/mol