题目内容
15.水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸和甲醇在酸性催化剂下合成水杨酸( )甲酯并计算其产率.实验步骤如下:
)甲酯并计算其产率.实验步骤如下:Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,以及约10mL甲苯(甲苯与
 水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
水形成的共沸物,其沸点为85℃;该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀后加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯5.3g.
常用物理常数如下:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)实验中加入沸石的作用是防暴沸;
(3)加入甲苯的作用是将反应产生的水从反应体系中分离出来,使合成水杨酸甲酯反应的化学平衡向右移动,从而提高反应的产率.
(4)反应结束后,分离甲醇所采用操作的名称是蒸馏.
(5)洗涤操作中,前后两次水洗的目的分别是为了洗掉洗掉大部分硫酸和洗掉碳酸氢钠.
(6)在蒸馏操作中,仪器选择及安装都正确的是(填标号)b.

(7)本实验的产率为70%(保留两位有效数字).
分析 Ⅰ.在浓硫酸作用下水杨酸和甲醇发生酯化反应生成水杨酸甲酯,发生酯化反应时生成水,水和甲苯能形成共沸物,从而易将水蒸出,使得平衡向右移动,水在低温下挥发,同时减少了甲醇的消耗,从而提高反应的产率;加热时加入沸石能防止溶液暴沸,从而减小安全事故的发生;发生酯化反应温度低于100℃,最好使用水浴加热,易控制温度;
Ⅱ.反应后的溶液要经过多次洗涤,在洗涤操作中,第一次水洗的主要目的是除去大部分催化剂硫酸,5%NaHCO3溶液既可以除去未洗净的硫酸,也可以降低酯的溶解度,但第二步洗涤后生成的酯中混有NaHCO3,所以第二次水洗,主要目的是除去产品中残留的碳酸氢钠;用硫酸镁吸收水分;
Ⅲ.互溶的液体应该采用蒸馏方法分离,所以将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯.
(1)仪器A的名称是冷凝管;水浴加热适用于降低温度的加热;
(2)沸石有防暴沸作用;
(3)甲苯和水能形成共沸物,使合成水杨酸甲酯反应的化学平衡向右移动,从而提高反应的产率;
(4)互溶的液体采用蒸馏方法分离;
(5)水能溶解可溶酸、碱、盐;
(6)蒸馏时,温度计测量馏分温度;
(7)先根据水杨酸和甲醇的物质的量,然后判断过量情况,根据不足量计算出理论上生成水杨酸甲酯的物质的量,最后根据实际上制取的水杨酸甲酯计算出产率.
解答 解:Ⅰ.在浓硫酸作用下水杨酸和甲醇发生酯化反应生成水杨酸甲酯,发生酯化反应时生成水,水和甲苯能形成共沸物,从而易将水蒸出,使得平衡向右移动,水在低温下挥发,同时减少了甲醇的消耗,从而提高反应的产率;加热时加入沸石能防止溶液暴沸,从而减小安全事故的发生;发生酯化反应温度低于100℃,最好使用水浴加热,易控制温度;
Ⅱ.反应后的溶液要经过多次洗涤,在洗涤操作中,第一次水洗的主要目的是除去大部分催化剂硫酸,5%NaHCO3溶液既可以除去未洗净的硫酸,也可以降低酯的溶解度,但第二步洗涤后生成的酯中混有NaHCO3,所以第二次水洗,主要目的是除去产品中残留的碳酸氢钠;用硫酸镁吸收水分;
Ⅲ.互溶的液体应该采用蒸馏方法分离,所以将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯.
(1)仪器A的名称是冷凝管;水浴加热适用于降低温度的加热,制取水杨酸甲酯所需温度低于100℃,最好使用水浴加热,易控制温度,故答案为:冷凝管;水浴加热;
(2)沸石有防暴沸作用,防止安全事故的发生,故答案为:防暴沸;
(3)水和甲苯能形成共沸物,从而易将水蒸出,使得平衡向右移动,水在低温下挥发,同时减少了甲醇的消耗,从而提高反应的产率,故答案为:反应产生的水;
(4)互溶的液体采用蒸馏方法分离,甲醇和水杨酸甲酯互溶,应该采用蒸馏方法分离,故答案为:蒸馏;
(5)反应后的溶液要经过多次洗涤,在洗涤操作中,第一次水洗的主要目的是除去大部分催化剂硫酸,5%NaHCO3溶液既可以除去未洗净的硫酸,也可以降低酯的溶解度,但第二步洗涤后生成的酯中混有NaHCO3,所以第二次水洗,主要目的是除去产品中残留的碳酸氢钠,故答案为:洗掉大部分硫酸;洗掉碳酸氢钠;
(6)蒸馏时,温度计测量馏分温度,只有b中温度计测量的是馏分温度,故选b;
(7)水杨酸和甲醇的物质的量分别为:0.05mol、0.75mol,由于水杨酸和甲醇是按照1:1进行反应,所以甲醇过量,生成水杨酸甲酯的量要按照水杨酸的物质的量计算,即理论上生成0.05mol水杨酸甲酯;实际上生成的水杨酸甲酯的质量为5.3g,物质的量为:$\frac{5.3g}{152g/mol}$=0.0349mol,所以实验中水杨酸甲酯的产率为$\frac{0.0349mol}{0.05mol}$×100%=70%,故答案为:70%.
点评 本题考查制备实验方案设计,为高频考点,涉及常见仪器的构造与安装、混合物的分离、提纯、物质的制取、物质产率的计算等知识,明确实验基本操作及各物质性质是解本题关键,难点是(5)中各洗涤剂的作用,题目难度中等.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案| A. | 3.01×1023 | B. | 5.32×1026 | C. | 6.02×1026 | D. | 1.2×1026 |
下列推断不合理的是( )
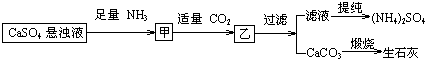
| A. | 通入CO2和NH3顺序可以颠倒 | |
| B. | 通入的NH3必须过量 | |
| C. | CO2可被循环使用 | |
| D. | 生成1mol(NH4)2SO4至少消耗2 mol NH3 |
(1)a>(填“>”、“=”或“<”)b.
(2)下表为不同温度下该反应的平衡常数.由此可推知,表中T1<(填“>”、“<”或“=”)T2.
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
(3)在相同条件下要得到2a KJ热量,加入各物质的物质的量可能是D.
A.4mol A2和2mol B2 B.4mol A2、2mol B2和2mol C3
C.4mol A2和4mol B2 D.6mol A2和4mol B2
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出C3气体 B.适当升高温度
C.增大B2的浓度 D.选择高效的催化剂
(5)若将上述容器改为恒压容器(反应前体积相同),起始时加入2mol A2和1mol B2,500℃时充分反应达到平衡后,放出热量d kJ,则d>(填“>”、“=”或“<”)b,理由是由于恒压容器中压强比恒容容器中的大,故反应物的转化率较高,生成C3比恒容时多,则放出的热量也多.
(6)在一定温度下,向一个容积不变的容器中通入2mol A2和1mol B2及适量固体催化剂,使反应达到平衡.保持同一反应温度,在相同容器中,将起始物质改为4mol A2、2mol B2,则平衡时A2的转化率变大(填“不变”、“变大”“变小”或“不能确定”).
| A. | 高分子化合物结构复杂,相对分子质量很大 | |
| B. | 对于一块高分子材料来说,n是一个整数,因而它的相对分子质量是确定的 | |
| C. | 高分子化合物是纯净物 | |
| D. | 高分子材料可分为天然高分子材料和合成高分子材料 |

 对叔丁基苯酚
对叔丁基苯酚 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下:反应物和产物的相关数据列表如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚.实验步骤如下:反应物和产物的相关数据列表如下: .该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是由于叔丁基氯挥发导致产率降低.
.该反应过于激烈,放出大量热,常使实验的产率降低,可能的原因是由于叔丁基氯挥发导致产率降低.