题目内容
15.Ⅰ恒温、恒压下,在一个可变容积的容器中发生如下反应:A(气)+B(气)?C(气)(1)若开始时放入1mol A和1mol B,到达平衡后,生成a mol C,这时A的物质的量为(1-a)mol,
(2)若开始时放入3mol A和3mol B,到达平衡后,生成C的物质的量为3amol.
(3)若开始时放入x mol A、2mol B和1mol C,到达平衡后,A和C的物质的量分别是y mol和3a mol,则x=2mol,y=3(1-a)mol.平衡时,B的物质的量(丁)(选填一个编号).
(甲)大于2mol (乙)等于2mol
(丙)小于2mol (丁)可能大于、等于或小于2mol
Ⅱ若维持温度不变,在一个与(Ⅰ)反应前起始体积相同、且容积固定的容器中发生上述反应.
(4)开始加入1mol A和1mol B 时A的转化率为m,若开始时加入1mol A和2mol B 时A的转化率为n,则m<n(“>”、“<”、“=”)
(5)开始时放入1 mol A和1mol B到达平衡后生成b mol C.将b与(1)小题中的a进行比较乙选填一个编号).
(甲)a<B<I>(乙)a>b (丙)a=b (丁)不能比较a和b的大小.
分析 I.(1)由方程式可知,由方程式可知△n(A)=$\frac{1}{2}$△n(C),平衡时A的物质的量=A的起始物质的量-△n(A);
(2)恒温恒压下,若开始时放入3mol A和3mol B,与(1)中A、B的物质的量之比均为1:1,则为等效平衡,平衡时反应物的转化率相同;
(3)若开始时放入x mol A,2mol B和1mol C,完全转化到左边满足3mol A和3mol B,与(1)中A、B的物质的量之比均为1:1,则为等效平衡,平衡时反应物的转化率相同,可以得到3amol C,平衡时A、B的物质的量分别为(1)中A、B的3倍,结合a<1判断;
Ⅱ.(4)恒温恒容下,开始加入1mol A和1mol B 时A的转化率为m,若开始时加入1mol A和2mol B等效为在前面平衡基础上再加入1mol,平衡正向移动;
(5)反应A(g)+B(g)?C(g)是气体体积减少的反应,在恒温恒容容器中,随反应进行压强减小,而在恒温恒压容器中随反应进行,过程中的压强为保持恒压,则本题的容器中的压力小于(1)小题容器中的压力,有利于逆向反应.
解答 解:I.(1)达到平衡后,生成a mol C,则△n(A)=△n(C)=amol,故A的物质的量为1mol-amol=(1-a)mol,故答案为:(1-a);
(2)恒温恒压下,若开始时放入3mol A和3mol B,与(1)中A、B的物质的量之比均为1:1,则为等效平衡,平衡时反应物的转化率相同,则平衡时生成C为(1)中的3倍,即生成C为3amol,故答案为:3a;
(3)若开始时放入x mol A,2mol B和1mol C,完全转化到左边满足3mol A和3mol B,与(1)中A、B的物质的量之比均为1:1,则为等效平衡,平衡时反应物的转化率相同,可以得到3amol C,1molC转化可以得到1molA、1molB,则x=3-1=2,则平衡时A为3(1-a)mol,平衡时B的物质的量为(1)中B的3倍,即为3(1-a)mol,由于0<a<1,故3(1-a)可能大于、等于或小于2,
故答案为:2;3(1-a);(丁);
Ⅱ.(4)恒温恒容下,开始加入1mol A和1mol B 时A的转化率为m,若开始时加入1mol A和2mol B等效为在前面平衡基础上再加入1mol,平衡正向移动,A的转化率增大,故m<n,
故答案为:<;
(5)在恒温恒压容器中开始时放入1molA和1molB到达平衡后生成amol C;在恒温恒容容器中开始时放入1molA和1molB到达平衡后生成b molC;反应A(g)+B(g)?C(g)是气体体积减少的反应,在恒温恒容容器中,随反应进行压强减小,在恒温恒压容器中随反应进行,过程中的压强为保持恒压,体积减小,所以本题的容器中的压力小于(1)小题容器中的压力,有利于逆向反应,因此平衡后a>b;
故答案为:乙.
点评 本题考查化学平衡有关计算、等效平衡问题,充分利用各步的隐含条件,依据等效平衡的特征分析是本题的关键,区分恒温恒容容器和恒温恒压容器的不同,难度较大.

| A. | 根据是否含氧元素,将物质分为氧化剂和还原剂 | |
| B. | 根据反应中是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 根据水溶液是否能够导电,将物质分为电解质和非电解质 | |
| D. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
| A. | Mn>Cu | B. | Al>Mn | C. | Mn>Mg | D. | Mn>H |
| A. | 大力发展太阳能和风力发电机可缓解电力紧张问题 | |
| B. | 将地沟油回收加工为燃料油,提高资源的利用率 | |
| C. | 推广使用一次性木筷,减少疾病传染 | |
| D. | 推广使用电动汽车、天然气汽车等环保公共交通工具 |

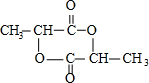 ;
; )在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:2n
)在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:2n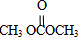 +n
+n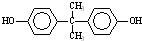 →
→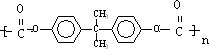 +4nCH3OH.
+4nCH3OH.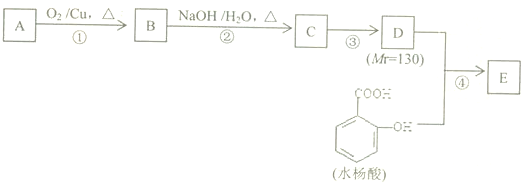
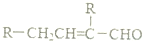
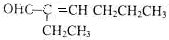 ,若要检验C中所含官能团,一次取样检验,按使用的先后顺序写出所用试剂用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键.
,若要检验C中所含官能团,一次取样检验,按使用的先后顺序写出所用试剂用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键. .
.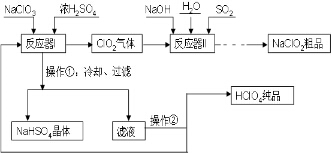 工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下:
工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下: 甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.
甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.