题目内容
12.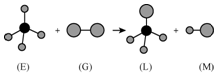 已知正四面体形分子E的直线型分子G反应,生成四面体形分子L和直线型分子M.组成E分子中的元素的原子序数都小于10,组成G分子的元素为第三周期的元素.如图,则下列判断中正确的是( )
已知正四面体形分子E的直线型分子G反应,生成四面体形分子L和直线型分子M.组成E分子中的元素的原子序数都小于10,组成G分子的元素为第三周期的元素.如图,则下列判断中正确的是( )| A. | 常温常压下,L是一种液态有机物 | B. | E是一种含有非极性键的分子 | ||
| C. | 干燥的G能漂白有色物质 | D. | 上述反应的类型是取 代反应 |
分析 正四面体形分子E,组成E分子的元素的原子序数都小于10,E由两种元素组成,体积小的球是H元素,体积大的球表示C元素,所以E是甲烷;直线型分子G,组成G分子的元素为第三周期的元素,且G是双原子分子,所以G是Cl元素,该反应是甲烷和氯气发生取代反应生成一氯甲烷和氯化氢,即L是一氯甲烷,M是氯化氢,据此分析.
解答 解:正四面体形分子E,组成E分子的元素的原子序数都小于10,E由两种元素组成,体积小的球是H元素,体积大的球表示C元素,所以E是甲烷;直线型分子G,组成G分子的元素为第三周期的元素,且G是双原子分子,所以G是Cl元素,该反应是甲烷和氯气发生取代反应生成一氯甲烷和氯化氢,即L是一氯甲烷,M是氯化氢.
A.常温常压下,L是一氯甲烷,一氯甲烷是气体,故A错误;
B.甲烷分子中只含碳氢键,属于极性共价键,故B错误;
C.氯气没有漂白性,但次氯酸有漂白,所以干燥的G不能漂白有色物质,故C错误;
D.甲烷中的氢原子被氯原子取代生成一氯甲烷,属于取代反应,故D正确;
故选D.
点评 本题以物质的推断为载体考查了元素化合物的性质、基本有机反应等知识点,能正确推断物质是解本题的关键,注意甲烷的氯代烃中只有一氯甲烷是气体,为易错点.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
3.元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语.下列有关化学用语的表示方法中错误的是( )
| A. | 次氯酸的电子式: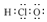 | B. | S2-的结构示意图: | ||
| C. | O-18的原子符号:${\;}_{\;}^{15}$O | D. | CO2分子的结构式:O=C=O |
20.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下一定呈气体 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 元素B的单质可被热的浓硫酸或浓硝酸氧化 | |
| D. | 化合物AE与CE含有相同类型的化学键 |
1.X、Y、Z是3种原子序数逐渐增大的短周期元素,其中X、Y位于同一主族,X原子的最外层电子数是其电子层数的3倍.下列说法正确的是( )
| A. | 元素非金属性由弱到强的顺序为Z<Y<X | |
| B. | 化合物YZ2中各原子都达到8电子结构 | |
| C. | 这3种元素的氢化物的沸点由高到低的顺序为:Z>Y>X | |
| D. | 其对应的阴离子半径由大到小的顺序为:Z>Y>X |
6.下列有关NO2的说法正确的是( )
| A. | NO2可由N2与O2反应直接制备 | |
| B. | NO2有毒,但因其易溶于水且与水反应,因此不属于大气污染物 | |
| C. | NO2既有氧化性也有还原性 | |
| D. | NO2为红棕色气体,因此将NO2通入水中,溶液显红棕色 |
 ⑤乙烷和丁烷
⑤乙烷和丁烷 将纯锌片和纯铜片按图所示方式插入同浓度的稀硫酸中请回答下列问题:
将纯锌片和纯铜片按图所示方式插入同浓度的稀硫酸中请回答下列问题: