题目内容
下列叙述正确的是( )
| A、常温下,78 g Na2O2中含有的阴离子数是2NA |
| B、标准状况下,22.4LSO3的物质的量为1mol |
| C、常温常压下,22.4 L SO2和O2混合气体中含有的氧原子数是2 NA |
| D、铁铝混合物与一定量稀盐酸反应生成1 mol H2时,转移电子数是2 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量,结合过氧化钠含有钠离子和过氧根离子构成分析;
B、标准状况三氧化硫不是气体;
C、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol;
D、依据氧化还原反应电子守恒计算分析.
| m |
| M |
B、标准状况三氧化硫不是气体;
C、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol;
D、依据氧化还原反应电子守恒计算分析.
解答:
解:A、依据n=
计算物质的量=
=1mol,结合过氧化钠含有钠离子和过氧根离子构成分析含有的阴离子数是NA,故A错误;
B、标准状况三氧化硫不是气体,22.4LSO3的物质的量不是1mol,故B错误;
C、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol,常温常压下,22.4 L SO2和O2混合气体物质的量不是1mol,故C错误;
D、氧化还原反应中电子守恒可知,H元素得到电子,反应生成1 mol H2时,电子转移2mol,转移电子数是2NA,故D正确;
故选D.
| m |
| M |
| 78g |
| 78g/mol |
B、标准状况三氧化硫不是气体,22.4LSO3的物质的量不是1mol,故B错误;
C、依据气体摩尔体积的条件分析判断,标准状况气体摩尔体积为22.4L/mol,常温常压下,22.4 L SO2和O2混合气体物质的量不是1mol,故C错误;
D、氧化还原反应中电子守恒可知,H元素得到电子,反应生成1 mol H2时,电子转移2mol,转移电子数是2NA,故D正确;
故选D.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件应用,注意反应电子转移计算,掌握基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法错误的是( )
| A、食醋用氢氧化钠溶液滴定开始时,溶液的PH通常变化缓慢,当接近完全反应时(即滴定终点),pH出现突变,称为滴定突跃 |
| B、纸层析法分离铁离子和铜离子实验中,点样后的滤纸晾干后将其末端浸入展开剂中约0.5cm |
| C、Cu2+与足量氨水反应的离子方程式 Cu2++2NH3?H2O═Cu(OH)2↓+2NH4+ |
| D、硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 |
用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
| A、常温常压下,22.4 L Cl2与足量的铁粉反应,转移的电子数目为2NA |
| B、常温常压下,4 g CH4含有NA个C-H键 |
| C、常温常压下,92 g的NO2和N2O4混合气体中含有的原子数目为6NA |
| D、分子总数为NA的SO2和CO2混合气体中含有的氧原子数目为2NA |
下列实验操作或原理不正确的是( )
| A、纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 |
| B、抽滤时,滤纸要小于布氏漏斗 |
| C、重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 |
| D、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
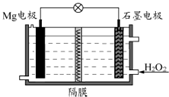 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法不正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法不正确的是( )| A、Mg 电极是该电池的负极 |
| B、H2O2 在石墨电极上发生还原反应 |
| C、石墨电极附近溶液的pH 增大 |
| D、溶液中Cl-向正极移动 |
下列溶液中的氯离子浓度与50mL0.1mol/L氯化铝溶液中的氯离子浓度相等的是( )
| A、150mL 0.1mol/L NaCl |
| B、75mL 0.2mol/L NH4Cl |
| C、100mL 0.3mol/L KCl |
| D、150mL 0.1mol/L FeCl3 |
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g).不能判断该分解反应已经达到化学平衡的是( )
| A、密闭容器中二氧化碳的体积分数不变 |
| B、密闭容器中气体的总物质的量不变 |
| C、密闭容器中混合气体的密度不变 |
| D、v(NH3)正=2 v(CO2)逆 |
下列涉及的有机物及有机反应类型正确的是( )
| A、乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应 |
| B、葡萄糖、蛋白质、纤维素都能发生水解反应 |
| C、苯乙烯,氯乙烯,乙二醇均可做加聚反应的单体 |
| D、苯与甲苯都是芳香烃,均可以使酸性高锰酸钾褪色 |
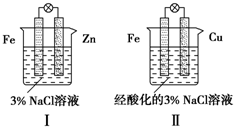 K3[Fe(CN)6]铁氰化钾,别名赤血盐,深红色或红色单斜晶系柱状结晶或粉未,有剧毒.遇亚铁盐生成蓝色沉淀.结合下图判断,下列叙述正确的是( )
K3[Fe(CN)6]铁氰化钾,别名赤血盐,深红色或红色单斜晶系柱状结晶或粉未,有剧毒.遇亚铁盐生成蓝色沉淀.结合下图判断,下列叙述正确的是( )| A、Ⅰ和Ⅱ中负极反应均是Fe-2e-═Fe2+ |
| B、Ⅰ和Ⅱ中正极均被保护 |
| C、Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e-═4OH- |
| D、Ⅰ和Ⅱ中分别加入少量K3[Fe(CN)6]溶液,均有蓝色沉淀 |