题目内容
5.观察与思考是学习科学知识的基本方法之一.家里用自来水养金鱼时,总要将自来水晾晒之后才加入鱼缸中.你知道这里面的奥妙吗?分析 普通的自来水在自来水厂都要通入氯气消毒,氯气和水反应生成盐酸和次氯酸,化学方程式:Cl2+H2O?HCl+HClO,HClO具有强氧化性,以此来解答.
解答 解:自来水在Cl2消毒中发生Cl2+H2O?HCl+HClO,HClO 具有强氧化性,能够破坏细菌的结构,从而杀死细菌,达到消毒目的,如果将刚从自来水龙头里放出来的水直接养鱼,里面的次氯酸和盐酸就会将鱼致死,放在阳光里晒一下就是为了将次氯酸分解和使盐酸挥发出去,发生2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,达到除去溶解在自来水中游离的氯气,防止金鱼中毒的目的,
故答案为:将次氯酸分解和使盐酸挥发出去,发生2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,除去溶解在自来水中游离的氯气,防止金鱼中毒.
点评 本题考查HClO的性质,为高考常见题型和高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.硝酸铵溶液中,离子浓度由大到小的顺序是( )
| A. | c(NH4+)>c(NO3-)>c(H+)>c(OH-) | B. | c(NO3-)>c(NH4+)>c(H+)>c(OH-) | ||
| C. | c(H+)>c(NH4+)>c(NO3-)>c(OH-) | D. | c(OH-)>c(NO3-)>c(NH4+)>c(H+) |
14.下列关于有机物因果关系的叙述中,完全正确的一组是( )
| 选项 | 原因 | 结论 |
| A | 乙烯和苯都能使溴水褪色 | 苯分子和乙烯分子含有相同的碳碳双键 |
| B | 乙酸分子中含有羧基 | 可与NaHCO3溶液反应生成CO2 |
| C | 乙醇是电解质 | 乙醇可与钠反应放出氢气 |
| D | 乙酸乙酯和乙烯在一定条件下都能与水反应 | 二者属于同一反应类型 |
| A. | A | B. | B | C. | C | D. | D |
10.如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是( )
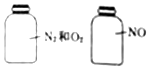

| A. | 摩尔质量相等 | B. | 气体密度相等 | C. | 气体质量相等 | D. | 所含分子数相等 |
17.表1是元素周期表的一部分:
表1
表2
25℃时,用浓度为0.1000mol/L的NaOH溶液分别滴定20.00mL浓度均为0.1000mol/L 的两种酸HX、HZ(忽略体积变化),实验数据如表2,下列判断正确的是( )
表1
| 氧 | X |
| Y | Z |
| 数据编号 | 滴入NaOH溶液的体积/mL | 溶液pH | |
| HX | HZ | ||
| ① | 0 | 3 | 1 |
| ② | 20.00 | a | 7 |
| A. | 表格中a<7 | |
| B. | HX和HZ等体积混合后pH=1+lg2 | |
| C. | Y和Z两元素的简单氢化物受热分解,前者分解温度高 | |
| D. | 0.l000 mol/L Na2Y的水溶液中:c(Y2-)+c(HY-)+c(H2Y)=0.1000 mol/L |
14.下列指定反应的离子方程式正确的是( )
| A. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 银氨溶液中滴加过量的盐酸:Ag(NH3)2++2H+═Ag++2NH4+ | |
| C. | 过量的铁粉与稀硝酸反应:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
2.一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(P分)=气体总压(P总)×体积分数.下列说法正确的是( )
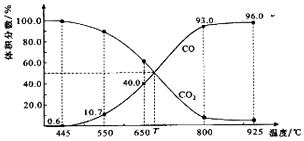

| A. | 550℃时,若充入惰性气体,v正、v逆均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 | |
| D. | 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.0P总 |