题目内容
19.配平氧化还原反应方程式:5 C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O.
分析 反应中草酸根离子中碳从+3价升高到二氧化碳中+4价,高锰酸根中+7及的锰降低到+2价,依据氧化还原反应得失电子守恒、原子个数守恒配平方程式,据此解答.
解答 解:反应中草酸根离子中碳从+3价升高到二氧化碳中+4价,高锰酸根中+7及的锰降低到+2价,要使得失电子守恒,则最小公倍数为10,草酸根离子系数为5,高锰酸根离子系数为2,依据原子个数守恒方程式为5 C2O42-+2MnO4-+16H+=10CO2+2Mn2++8H2O,
故答案为:5;2; 16;10;2;8.
点评 本题考查了氧化还原反应方程式的书写,准确把握反应中各元素化合价变化,明确氧化还原反应得失电子守恒是解题关键,题目难度不大.

练习册系列答案
相关题目
9.已知C-C键可以绕键轴自由旋转,结构简式为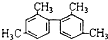 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )
 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )| A. | 分子中至少有9个碳原子处于同一平面上 | |
| B. | 分子中至少有11个碳原子处于同一平面上 | |
| C. | 该有机物不能使酸性KMnO4溶液褪色 | |
| D. | 该烃属于苯的同系物 |
4.下列对有关化学反应过程或实验现象的解释正确的是( )
| A. | Cl2的水溶液可以导电,说明Cl2是电解质 | |
| B. | 某溶液中加入硝酸酸化的氯化钡溶液有白色沉淀生成说明溶液中一定含有SO42- | |
| C. | 向淀粉碘化钾的溶液中加入氯水,溶液变为蓝色,说明Cl2的氧化性强于I2 | |
| D. | 切开金属钠暴露在空气中,光亮表面逐渐变暗2Na+O2=Na2O2 |
8.下列根据实验现象得出的结论正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 废FeCl3蚀刻液中加入少量铁粉、振荡 | 得到澄清溶液 | 蚀刻液中一定不含Cu2+ |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | 稀硫酸能氧化Fe2+ |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2,充分振荡,静置 | 有机相呈现橙色 | 氧化性:Cl2>Br2 |
| D | 葡萄糖溶液与新制Cu(OH)2混合加热 | 生成砖红色沉淀 | 葡萄糖分子中含有醛基 |
| A. | A | B. | B | C. | C | D. | D |

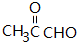 .
.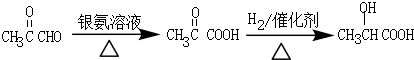 .
.