题目内容
14.25℃、pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA.× (判断对错)分析 根据PH=-lg[H+]、[H+][OH-]=Kw、n=cV来计算;
解答 解:pH=13的 Ba(OH)2溶液,[H+]=10-13mol/L,依据[H+][OH-]=Kw,[OH-]=10-1mol/L,25℃、pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为10-1mol/L×1L=0.1mol,含有的OH-数目为0.1NA,故错误.
点评 本题考查了有关物质的量计算,熟悉pH计算公式、水的离子积常数是解题关键,题目难度不大.

练习册系列答案
相关题目
5.由氧原子组成的另外一种分子化学式为O3.1mol O3和1mol O2具有相同的( )
| A. | 分子数 | B. | 原子数 | C. | 质子数 | D. | 电子数 |
6.下列离子在给定条件下,可能大量共存的是( )
| A. | 某无色透明的溶液中:Ca2+、NH4+、CO32-、HCOO- | |
| B. | 溶解有AlCl3的溶液中:Na+、K+、SO42-、S2- | |
| C. | 25℃时,水电离出的c(H+)=1×l0-l3mol/L的溶液中:K+、Ba2+、NO3-、I- | |
| D. | 离子浓度均为0.1mol/L的溶液中:Na+、Fe3+、CH3COO-、NO3- |
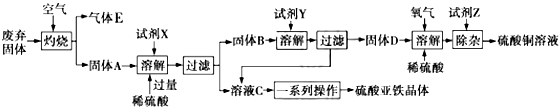
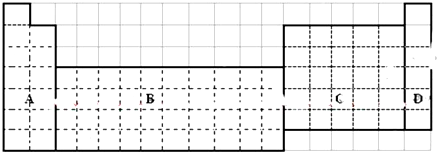
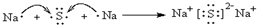 .
.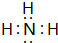 ,请用电子式表示A与C形成化合物的过程
,请用电子式表示A与C形成化合物的过程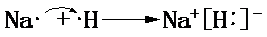 .
.