��Ŀ����
��1������
| ���ʣ����ʣ� | ��ȥ���� �����Լ��� | ���ӷ���ʽ ���������ӷ���ʽ����д��ѧ����ʽ�� |
| Fe(Al) | | |
| SiO2��CaCO3�� | | |
| CO2(HCl) | | |
| NaHCO3��Һ��Na2CO3�� | | |
| Na2CO3��NaHCO3�� | | |
| Al2O3��Al(OH)3�� | | |
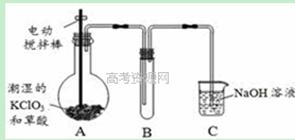
��2������������ͨ�뵽�Ȼ�����Һ��δ��������������ͨ�������Һ�еμ���ˮ��ˮ����������ɫ�����������ó����ijɷֱַ�Ϊ �� ����ֱ�д��������Ӧ�����ӷ���ʽ �� ��
��15�֣���1�����ʣ����ʣ� ��ȥ���������Լ� ���ӷ���ʽ Fe��Al�� ����������Һ 2Al+ 2OH��+ 2H2O=AlO2��+ 3H2�� SiO2��CaCO3�� ���� CaCO3+ 2H+= Ca2+ + CO2��+ H2O CO2��HCl�� ����̼��������Һ HCO3��+ H+=H2O+ CO2�� NaHCO3��Һ��Na2CO3�� CO2 CO32��+ CO2+ H2O=2HCO3�� Na2CO3��NaHCO3�� ����������Һ
�����HCO3��+ OH��=CO32��+ H2O
��2NaHCO3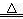 Na2CO3+CO2��+ H2O
Na2CO3+CO2��+ H2OAl2O3��Al(OH)3�� ���� 2Al(OH)3 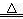 Al2O3+3H2O
Al2O3+3H2O
��2��BaSO4 BaSO3 Ba2++SO2+Cl2+2H2O=BaSO4��+4H++2Cl��
Ba2++2NH3+H2O+SO2=BaSO3��+2NH4+
���������������1�����������ǽ����˳�������ǰ��������������ϡ���ᣬ��������������������Һ����������������������Һ������ƫ�����ƺ��������������������Һ���Գ�ȥ���л�������������������費����ˮ�����ᣬ̼���������ˮ�����������ᣬ�����Ȼ��ơ�������̼��ˮ�����������Գ�ȥ���������л����̼��ƣ�������̼������̼�����Ʒ�Ӧ�����ܽ�Ƚ�С�������ڱ���̼�����ƣ��Ȼ�����ܽ�Ƚϴ������ڱ���̼�����ƣ�����֮��Ӧ�����Ȼ��ơ�������̼��ˮ����˿��ñ���̼��������Һ��ȥCO2�л����HCl��CO2��Na2CO3��Һ�ܷ�Ӧ����NaHCO3����˿���ͨ������CO2�����ȥ̼��������Һ�л��е�̼���ƣ�̼�����ƿ���ת��Ϊ̼���ƣ�����������NaOH�к�̼�����ƣ������ȣ�ʹ���ȶ���̼�����Ʒֽ�Ϊ̼���ơ�������̼��ˮ���������ȶ����������������ֽ�Ϊ��������ˮ����2��������������л�ԭ�ԣ�Ҳ���������������ͨ�ԣ���ˮ������SO2��NH3���к�SO2��ǰ�߳��ְ�ɫ������ԭ����SO2+Cl2+2H2O=4H++2Cl��+SO42����Ba2++SO42��=BaSO4�������ߵ�ԭ����SO2+2NH3+2H2O=2NH4++SO32����Ba2++SO32��=BaSO4����
���㣺��������ķ������ᴿ�����ӷ���ʽ��ѧ����ʽ����д������������������������̼���ơ�̼�����ơ��������衢̼��ơ�HCl���������������������������Ρ��������ε���Ҫ��ѧ���ʵ����֪ʶ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�ij�����Һ�п��ܺ��е��������±���ʾ��
| ���ܴ������е������� | H+��Ag+��Mg2+��Al3+��NH ��Fe3+ ��Fe3+ |
| ���ܴ������е������� | Cl-��Br-��I-��CO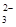 ��AlO ��AlO |
Ϊ̽����ɷ֣�����������̽��ʵ�顣
��1��̽��һ��
��ͬѧȡһ�����Ļ����Һ����������μ�������������Һ���������������ʵ���(n)��������� ������Һ�������V���Ĺ�ϵ��ͼ��ʾ��
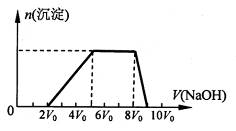
�ٸ���Һ��һ�����е���������______________�����Ӧ���ʵ���Ũ��֮��Ϊ________��һ�������ڵ���������_____________��
����д���������ٹ����з�����Ӧ�����ӷ���ʽ_____________________________��
��2��̽������
��ͬѧ������Һ�к��д�����Cl-��Br-��I-������1 L�û����Һ��ͨ��һ������Cl2����Һ��Cl-��Br-��I-�����ʵ�����ͨ��Cl2���������״�����Ĺ�ϵ���±���ʾ�� ������ش��������⣺
| Cl2���������״���� | 5.6 L | 11.2 L | 22.4 L |
| n (Cl-) | 2.5 mol | 3.0 mol | 4.0 mol |
| n (Br-) | 3.0 mol | 2.8 mol | 1.8 mol |
| n (I-) | x mol | 0 | 0 |
�ٵ�ͨ��Cl2�����Ϊ5.6 Lʱ����Һ�з�����Ӧ�����ӷ���ʽΪ_______________��
��ԭ��Һ��Cl-��Br-��I-�����ʵ���Ũ��֮��Ϊ______________________��
ij��ɫ��Һ�������п��ܴ����������ӣ�Na+��Ag+��Ba2+��Al3+��AlO2-��S2-��CO32-��SO32-��SO42-����ȡ����Һ�����й����飬�������£�
�ش��������⣺
��1�����ɳ��������ӷ���ʽ�� ��
��֪�������������������ɣ�������ˮ������HBr�����������ʵ����һ���������ֳɷ֣��������Լ��Լ����������±��У��ɲ�����������ÿһ�ж�Ӧ��ȷ���ɵ÷֣�
| ���� | ʵ��Ŀ�� | �Լ� | ���� |
| 1 | | | |
| 2 | | | |
| 3 | | | |
| 4 | | | |
��2������Һ�����ɳ����ҵ����ӷ���ʽ�� ��
��3����������������Һ�п϶����ڵ������У� ��
��4�������Һ�п��ܴ��ڵ����ӣ���ʵ����֤���Ƿ���ڵķ�����
��
��һ�����������������������ɵ��γ�Ϊ���Ρ�����CaOCl2��������Һ�п��Է�����Ӧ����Cl2�����й��ڻ���CaOCl2���й��жϲ���ȷ���ǣ�NAΪ�����ӵ�����)
| A���û�����������Һ�в���1mol Cl2ʱת�Ƶĵ�����ΪNA |
| B���û��ε�ˮ��Һ����Ư���� |
| C���û�������Ԫ�صĻ��ϼ�Ϊ+1��-1�� |
| D���û��ξ��н�ǿ�Ļ�ԭ�� |

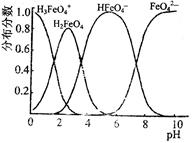
 4Fe(OH)3����8OH��+3O2��,��K2FeO4������ˮ�����е������� ��
4Fe(OH)3����8OH��+3O2��,��K2FeO4������ˮ�����е������� ��