题目内容
13.在100mL葡萄糖溶液中含有1.204×1023个葡萄糖分子,溶质的物质的量浓度为2mol•L-1.分析 先根据n=$\frac{N}{{N}_{A}}$计算出1.204×1023个葡萄糖分子的物质的量,然后根据c=$\frac{n}{V}$计算出该溶液的物质的量浓度.
解答 解:1.204×1023个葡萄糖分子的物质的量为:n=$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}}$=0.2mol,
该溶液中葡萄糖的物质的量浓度为:c=$\frac{0.2mol}{0.1L}$=2mol/L,
故答案为:2.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量与阿伏伽德罗常数之间的关系为解答结构,注意掌握物质的量浓度的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列各组物质中,互为同素异形体的是( )
| A. | CH4和CH3CH3 | B. | 11H和 12H | C. | O2和O3 | D. | D2O和T2O |
4.根据碳四价、氧二价、氢一价、氮三价的原则,可能成立的分子式是( )
| A. | C4H4 | B. | C7H15O | C. | C3H9O | D. | C4H7NO |
8.下列叙述正确是(用NA 代表阿伏加德罗常数的值)( )
| A. | 2.4g 金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 1mol甲烷分子所含质子数为10NA | |
| C. | 常温常压下,2g氢气含有的分子与32g氧气中分子数目均为NA | |
| D. | 4g氦气所含原子数为2NA |
7.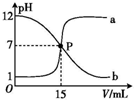 曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )
曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )
 曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )
曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )| A. | 盐酸的物质的量浓度与 NaOH 溶液的物质的量浓度相等 | |
| B. | P 点时溶液中 c(Na+)=c(Cl-)=c(H+)=c(OH-) | |
| C. | 曲线 a 是盐酸滴定氢氧化钠溶液的滴定曲线 | |
| D. | 曲线 b 中滴定前 NaOH 溶液的体积为 150 mL |
 R可以被KMnO4的酸性溶液氧化生成
R可以被KMnO4的酸性溶液氧化生成 COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到 COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为
COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为 COOH的异构体共有7种,其中的3种是:
COOH的异构体共有7种,其中的3种是: CH2CH2CH2CH2CH3,
CH2CH2CH2CH2CH3,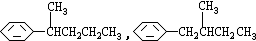
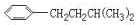 ,
,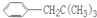 ,
,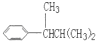 ,
, .
.