题目内容
7.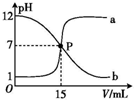 曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )
曲线 a 和 b 是常温下盐酸与氢氧化钠溶液相互滴定的滴定曲线.下列叙述中正确的是( )| A. | 盐酸的物质的量浓度与 NaOH 溶液的物质的量浓度相等 | |
| B. | P 点时溶液中 c(Na+)=c(Cl-)=c(H+)=c(OH-) | |
| C. | 曲线 a 是盐酸滴定氢氧化钠溶液的滴定曲线 | |
| D. | 曲线 b 中滴定前 NaOH 溶液的体积为 150 mL |
分析 曲线a的pH是由小到大,说明是氢氧化钠溶液滴定盐酸溶液的曲线;曲线b的pH由大到小,说明是盐酸滴定氢氧化钠溶液;曲线b可知NaOH溶液的pH=12,则氢氧化钠溶液的浓度为:(NaOH)=0.01mol/L;曲线a中盐酸溶液的pH=1,pH=-lgc(H+)=1,则c(HCl)=c(H+)=0.1mol/L;P点溶液的pH=7,呈中性,则c(Na+)=c(Cl-)、c(H+)=c(OH-),溶液中氢离子和氢氧根离子浓度很小,则P点离子浓度大小为:c(Na+)=c(Cl-)>c(H+)=c(OH-);曲线b中P点消耗15mL盐酸,则氢氧化钠溶液的体积为:$\frac{0.1mol/L×0.015L}{0.01mol/L}$=0.15L=150mL,据此进行解答.
解答 解:A.曲线b可知NaOH溶液的pH=12,则氢氧化钠溶液的浓度为:(NaOH)=0.01mol/L;曲线a中盐酸溶液的pH=1,则c(HCl)=c(H+)=0.1mol/L,两溶液浓度不相等,故A错误;
B.P点溶液的pH=7,呈中性,则c(Na+)=c(Cl-)、c(H+)=c(OH-),溶液中氢离子和氢氧根离子浓度很小,则P点离子浓度大小为:c(Na+)=c(Cl-)>c(H+)=c(OH-),故B错误;
C.曲线a的pH是由小到大,说明是氢氧化钠溶液滴定盐酸溶液的曲线,故C错误;
D.曲线b中P点消耗15mL盐酸,则氢氧化钠溶液的体积为:$\frac{0.1mol/L×0.015L}{0.01mol/L}$=0.15L=150mL,故D正确;
故选D.
点评 本题考查中和滴定、溶液中离子浓度大小比较,题目难度中等,试题借助于滴定曲线考查了中和滴定过程中PH的变化,注意掌握比较溶液中离子浓度大小的方法.

 阅读快车系列答案
阅读快车系列答案| 编号 | 电极材料 | 电解质溶液 | 灵敏电流计指针偏转方向 |
| 1 | Mg Al | 稀盐酸 | 偏向Al |
| 2 | Al Cu | 稀盐酸 | 偏向Cu |
| 3 | Al 石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg Al | NaOH溶液 | 偏向Mg |
| 5 | Al Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所作的电极是否相同?否(用“是”或“否”回答);
(2)写出实验3中的电极名称和电极反应式:
铝为负极极,2Al-6e-═2Al3+;
石墨为正极,6H++6e-═3H2↑(;
(3)实验4中的铝为负极,写出电池总反应方程式2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
(4)解释实验5中灵敏电流计指针偏向铝的原因:Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电子由负极流向正极,所以电流计指针偏向铝
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受哪些因素的影响?自发的氧化还原反应中金属铝是否参与反应,金属铝参加反应,失电子,做负极,反之作正极,与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关.
| A. | Al、Si、P | B. | I、Br、Cl | C. | O、S、Na | D. | Na、Mg、Ba |
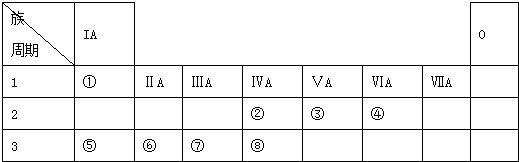
| 编号 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径/10-10m | 0.77 | 0.99 | 1.86 | 0.75 | 1.17 | 1.02 | 1.43 | 0.71 | 1.52 | 0.89 |
| 最高正化合价 | +4 | +7 | +1 | +5 | +4 | +6 | +3 | +1 | +2 | |
| 最低负化合价 | -4 | -1 | -3 | -4 | -2 | -1 |
(1)②和⑧两元素所对应的氢化物,最稳定的是HF(填化学式);
(2)③和⑥两元素的最高价氧化物对应水化物的反应是放热(填“放热”或“吸热”)反应;
(3)①⑤⑦三种元素的最高价氧化物对应水化物,酸性由强到弱的顺序是H2CO3>H2SiO3>Al(OH)3(填化学式).
| A. | H2、D2和T2互称为同素异形体 | B. | 35Cl和37Cl 互称为同位素 | ||
| C. |  和 和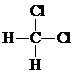 互称为同分异构体 互称为同分异构体 | D. | C2H4与C4H8一定能互称为同系物 |
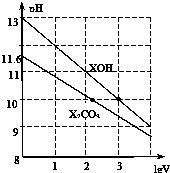 体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )| A. | XOH是强碱 | |
| B. | pH=10的两种溶液中的c(X+):XOH大于X2CO3 | |
| C. | 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1×10-10•2 | |
| D. | 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$减小 |
| A. | 该物质一定是钠的化合物 | B. | 该物质一定是金属钠 | ||
| C. | 该物质一定含钠元素 | D. | 可确定该物质中不含钾元素 |
 .
.