题目内容
1.10g重水(D2O)含0.5mol的D2O分子,含5mol中子,约含氧原子0.5NA个.分析 1个D2O分子中含中子数为:1×2+8=10,其摩尔质量为20g/mol,根据n=$\frac{m}{M}$计算出10g重水的物质的量,然后计算出含有氧原子的数目.
解答 解:10g重水(D2O)的物质的量为:n(D2O)=$\frac{10g}{20g/mol}$=0.5mol;
0.5mol D2O中含有中子的物质的量为:0.5mol×10=5mol;
0.5mol D2O中含有0.5molO原子,含有0.5NA个氧原子,
故答案为:0.5;5;0.5NA.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的化学计算能力.

练习册系列答案
相关题目
11.下列属于强电解质,且能导电的是( )
| A. | 饱和食盐水 | B. | KNO3固体 | C. | 熔融的NaOH | D. | HCOOH |
12.某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极是否相同?否(用“是”或“否”回答);
(2)写出实验3中的电极名称和电极反应式:
铝为负极极,2Al-6e-═2Al3+;
石墨为正极,6H++6e-═3H2↑(;
(3)实验4中的铝为负极,写出电池总反应方程式2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
(4)解释实验5中灵敏电流计指针偏向铝的原因:Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电子由负极流向正极,所以电流计指针偏向铝
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受哪些因素的影响?自发的氧化还原反应中金属铝是否参与反应,金属铝参加反应,失电子,做负极,反之作正极,与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关.
| 编号 | 电极材料 | 电解质溶液 | 灵敏电流计指针偏转方向 |
| 1 | Mg Al | 稀盐酸 | 偏向Al |
| 2 | Al Cu | 稀盐酸 | 偏向Cu |
| 3 | Al 石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg Al | NaOH溶液 | 偏向Mg |
| 5 | Al Zn | 浓硝酸 | 偏向Al |
(1)实验1、2中Al所作的电极是否相同?否(用“是”或“否”回答);
(2)写出实验3中的电极名称和电极反应式:
铝为负极极,2Al-6e-═2Al3+;
石墨为正极,6H++6e-═3H2↑(;
(3)实验4中的铝为负极,写出电池总反应方程式2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑
(4)解释实验5中灵敏电流计指针偏向铝的原因:Al遇浓硝酸发生钝化,发生Zn与浓硝酸的氧化还原反应,Zn作负极,Al作正极,电子由负极流向正极,所以电流计指针偏向铝
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受哪些因素的影响?自发的氧化还原反应中金属铝是否参与反应,金属铝参加反应,失电子,做负极,反之作正极,与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关.
16.下列反应中,在高温下不能自发进行的是( )
| A. | MgCO3(s)═MgO(s)+CO2(g) | B. | 2N2O5(g)?4NO2(g)+O2(g) | ||
| C. | (NH4)2CO3(s)?NH3(g)+NH4HCO3(s) | D. | 2CO(g)?2C(s)+O2(g) |
6.118号元素曾经被视为元素周期表的尽头,若118号元素的某种原子记作118297X,下列有关该核素的说法中,正确的是( )
| A. | 质子数为118,电子数为179,中子数为179 | |
| B. | 原子序数为179,质量数为297 | |
| C. | 与612C的相对原子质量之比为118:6 | |
| D. | 118297X经过一次α衰变得到的116号元素原子可表示116293X |
16.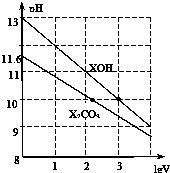 体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
 体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液分别加水稀释至体积为V,pH随lgV的变化情况如图所示,下列叙述中正确的是( )| A. | XOH是强碱 | |
| B. | pH=10的两种溶液中的c(X+):XOH大于X2CO3 | |
| C. | 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1×10-10•2 | |
| D. | 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$减小 |
 或
或 .
.
 .
.