题目内容
12.用氟硼酸(HBF4,属于强酸)代替硫酸作铅蓄电池的电解质溶液,可使铅蓄电池在低温下工作时的性能更优良,化学反应方程式为:Pb+PbO2+4HBF4$?_{充电}^{放电}$2Pb(BF4)2+2H2O,Pb(BF4)2为可溶于水的强电解质,下列说法正确的是( )| A. | 放电时,负极反应为:PbO2+4H++2e-=Pb2++2H2O | |
| B. | 充电时,当阳极质量增加23.9g时转移0.4mol电子 | |
| C. | 放电时,正极区电解质溶液的pH增大 | |
| D. | 充电时,Pb电极与电源的正极相连 |
分析 A.放电时,负极上发生失电子的氧化反应;
B.充电时阳极发生氧化反应:Pb2++2H2O-2e-═PbO2+4H+,根据关系式计算;
C.放电时正极上发生还原反应,根据电极反应式来判断;
D.电池在充电时,负极和电源的负极相连,正极和正极相连.
解答 解:A.放电时,负极上应该是金属铅发生失电子的氧化反应,不是还原反应,故A错误;
B.充电时阳极发生氧化反应Pb2++2H2O-2e-═PbO2+4H+,产生1molPbO2,增重1mol×239g/mol=239g,转移电子2mol,阳极质量增加23.9g时转移0.2mol电子,故B错误;
C.放电时正极上发生还原反应,PbO2+4H++2e-═Pb2++2H2O,氢离子浓度减小,所以pH增大,故C正确;
D.充电时,Pb电极和电源的负极相连,故D错误;
故选:C.
点评 本题考查了原电池与电解池原理的应用,根据元素化合价变化确定电极,再结合电极反应式来分析解答,难度中等,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
10.下列说法正确的是( )
| A. | 糖类、油脂、蛋白质、乙酸都能发生水解反应 | |
| B. | 糖类、油脂、蛋白质都是只由C、H、0三种元素组成的 | |
| C. | 糖类、油脂、蛋白质都是天然高分子化合物 | |
| D. | 油脂有油和脂肪之分,但都属于酯 |
4.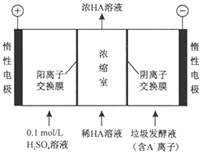 对生活污水进行处理是防止水体污染、改善水质的主要措施.电渗析法处理厨房垃圾发酵液(含污染物乳酸跟离子)同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).下列叙述中正确的是( )
对生活污水进行处理是防止水体污染、改善水质的主要措施.电渗析法处理厨房垃圾发酵液(含污染物乳酸跟离子)同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).下列叙述中正确的是( )
 对生活污水进行处理是防止水体污染、改善水质的主要措施.电渗析法处理厨房垃圾发酵液(含污染物乳酸跟离子)同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).下列叙述中正确的是( )
对生活污水进行处理是防止水体污染、改善水质的主要措施.电渗析法处理厨房垃圾发酵液(含污染物乳酸跟离子)同时得到乳酸的原理如图所示(图中“HA”表示乳酸分子,A-表示乳酸根离子).下列叙述中正确的是( )| A. | 阴极区溶液的pH变小 | |
| B. | 阳极的电极反应式为2H2O-4e-═4H++O2↑ | |
| C. | 通过一段时间后浓缩至水的量减少,导致乳酸溶液浓度上升 | |
| D. | 若阳、阴离子交换膜调换位置,与如图可以达到相同的效果 |
2.化学与生产、生活、社会密切相关.下列说法中正确的是( )
| A. | 煤的液化是物理变化 | |
| B. | 纤维素水解产物可以通过一系列化学变化制乙醇 | |
| C. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| D. | 漂白粉长期放置会被空气中的氧气氧化而变质 |
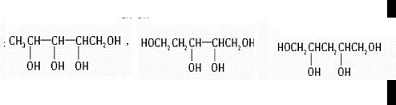
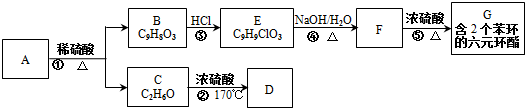
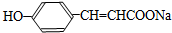 .
.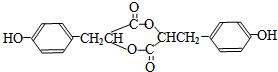 .
.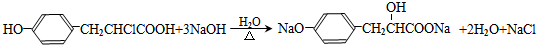 :反应①:
:反应①: .
.