题目内容
用图所示装置进行实验,不能达到实验目的是( )
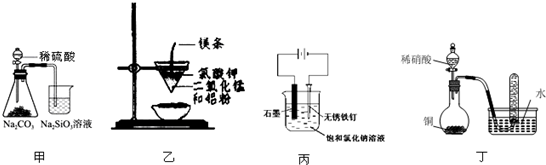

| A、用甲装置比较硫、碳、硅三种元素的非金属性强弱 |
| B、用乙装置可制得金属锰,用同样的装置可制得金属铬 |
| C、用丙装置可实现对铁钉的保护 |
| D、用丁装置验证铜与稀硝酸反应的气体产物只有NO |
考点:化学实验方案的评价,非金属在元素周期表中的位置及其性质递变的规律,金属的电化学腐蚀与防护,氮的氧化物的性质及其对环境的影响,探究铝热反应
专题:实验评价题
分析:A.元素的非金属性越强,其最高价氧化物的水化物酸性越强;
B.铝具有强还原性,能和部分金属氧化物发生铝热反应;
C.作电解池阴极的金属被保护;
D.要检验生成的气体中只含NO,要排除氧气的干扰.
B.铝具有强还原性,能和部分金属氧化物发生铝热反应;
C.作电解池阴极的金属被保护;
D.要检验生成的气体中只含NO,要排除氧气的干扰.
解答:
解:A.元素的非金属性越强,其最高价氧化物的水化物酸性越强,稀硫酸和碳酸钠反应生成二氧化碳,二氧化碳、水和硅酸钠反应生成硅酸,所以酸性:硫酸>碳酸>硅酸,则非金属性S>C>Si,故A正确;
B.铝具有强还原性,能和部分金属氧化物发生铝热反应而还原出金属单质,如Mn、Cr等,故B正确;
C.作电解池阴极的金属被保护,铁作电解池阴极被保护,故C正确;
D.要检验生成的气体中只含NO,要排除氧气的干扰,该装置中有氧气,NO易被氧化生成二氧化氮,所以对实验造成干扰,故D错误;
故选D.
B.铝具有强还原性,能和部分金属氧化物发生铝热反应而还原出金属单质,如Mn、Cr等,故B正确;
C.作电解池阴极的金属被保护,铁作电解池阴极被保护,故C正确;
D.要检验生成的气体中只含NO,要排除氧气的干扰,该装置中有氧气,NO易被氧化生成二氧化氮,所以对实验造成干扰,故D错误;
故选D.
点评:本题考查了实验方案评价,为高考热点,明确实验原理是解本题关键,根据物质的性质分析解答,注意D中可以采用 该装置验证铜和稀硝酸反应产生的气体,题目难度中等.
该装置验证铜和稀硝酸反应产生的气体,题目难度中等.
 该装置验证铜和稀硝酸反应产生的气体,题目难度中等.
该装置验证铜和稀硝酸反应产生的气体,题目难度中等.
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在11g由D和18O组成的水中,含中子数为(NA表示阿伏加德罗常数)( )
| A、NA |
| B、2NA |
| C、6NA |
| D、10NA |
下列实验能达到目的是( )
A、 除去乙烷中的乙烯 |
B、 制取蒸馏水 |
C、 乙醇催化氧化 |
D、 CO2喷泉实验 |
下列现象或事实可用同一原理解释的是( )
| A、氯水和二氧化硫使品红溶液褪色 |
| B、亚硫酸钠和水玻璃长期暴露在空气中变质 |
| C、稀硝酸和三氯化铁溶液使KI-淀粉试纸变蓝 |
| D、浓盐酸和浓硫酸长期暴露在空气中浓度变小 |
下列热化学方程式正确的是( )
| A、S(s)+O2(g)═SO2(g);△H=-269.8kJ/mol |
| B、NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.3kJ/mol |
| C、表示乙醇的燃烧热:C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol |
| D、2NO2═O2+2NO;△H=+116.2kJ/mol |
下列说法符合绿色化学思想的是( )
| A、对工业生产硝酸产生的废气、废水进行严格处理 |
| B、利用根瘤菌固氮以减少氮肥生产厂 |
| C、实验室制备NO2时在通风橱内进行 |
| D、建设“花园式工厂” |
 实验室制取乙炔的实验装置图(如图)中,
实验室制取乙炔的实验装置图(如图)中,