题目内容
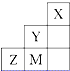
如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )

| A、电负性:Y>Z>M |
| B、离子半径:M->Z2->Y- |
| C、ZM2分子中各原子的最外层均满足8电子稳定结构 |
D、Z元素基态原子最外层电子排布图为 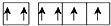 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:图为元素周期表中短周期的一部分,由Y、Z、M在周期表中的位置关系可知,Y为F元素,M为Cl元素,Z为S元素.
A、同周期自左而右非金属性增强,同主族自上而下非金属性减弱,元素的非金属性越强,其电负性越大;
B、电子层排布相同,核电荷数越大离子半径越小,最外层电子数相同,电子层越多离子半径越大;
C、ZM2为SCl2,分子中S元素化合价为+2价,Cl元素化合价为-1价,原子最外层电子数+化合价绝对值=8,满足8电子稳定结构;
D、电子排布符合洪特规则.
A、同周期自左而右非金属性增强,同主族自上而下非金属性减弱,元素的非金属性越强,其电负性越大;
B、电子层排布相同,核电荷数越大离子半径越小,最外层电子数相同,电子层越多离子半径越大;
C、ZM2为SCl2,分子中S元素化合价为+2价,Cl元素化合价为-1价,原子最外层电子数+化合价绝对值=8,满足8电子稳定结构;
D、电子排布符合洪特规则.
解答:
解:图为元素周期表中短周期的一部分,由Y、Z、M在周期表中的位置关系可知,Y为F元素,M为Cl元素,Z为S元素.
A、同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性:Y>M>Z,故电负性Y>M>Z,故A错误;
B、电子层排布相同,核电荷数越大离子半径越小,最外层电子数相同,电子层越多离子半径越大,离子半径:Z2->M->Y-,故B错误;
C、ZM2为SCl2,分子中S元素化合价为+2价,2+6=8,S原子满足8电子稳定结构,Cl元素化合价为-1价,|-1|+7=8,Cl原子满足8电子稳定结构,故C正确;
D、不同轨道的单电子自旋方向不同,违反了洪特规则,故D错误.
故选C.
A、同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性:Y>M>Z,故电负性Y>M>Z,故A错误;
B、电子层排布相同,核电荷数越大离子半径越小,最外层电子数相同,电子层越多离子半径越大,离子半径:Z2->M->Y-,故B错误;
C、ZM2为SCl2,分子中S元素化合价为+2价,2+6=8,S原子满足8电子稳定结构,Cl元素化合价为-1价,|-1|+7=8,Cl原子满足8电子稳定结构,故C正确;
D、不同轨道的单电子自旋方向不同,违反了洪特规则,故D错误.
故选C.
点评:本题考查元素周期表、元素周期律、半径比较、分子结构等,注意整体把握元素周期表,掌握元素周期律.

练习册系列答案
相关题目
下列化学用语的表达正确的是( )
A、Na2SO4电离:Na2SO4=Na2++SO
| ||
B、Cl-的结构示意图: | ||
C、质子数为6,中子数为8的微粒:
| ||
| D、医用“钡餐”的化学式:BaSO4 |
将Al片投入某无色澄清溶液中,产生大量H2,则该溶液中可能含有的微粒是( )
| A、K+、OH-、NO3-、Cl- |
| B、H+、Na+、CO32-、Cl- |
| C、H+、K+、NO3-、Cl- |
| D、Cu2+、H+、Cl-、SO42- |
下列叙述错误的是( )
| A、制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
| B、SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、用AgNO3溶液可以鉴别KCl和KI |
0.03molCu投入到一定量的浓HNO3 中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2 的体积为( )
| A、504mL |
| B、336mL |
| C、224mL |
| D、168mL |
常温下,若溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2mL混合而得,则下列说法正确的是 ( )
| A、若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol?L-1 |
| B、若V1=V2,反应后溶液的pH一定等于7 |
| C、若反应后溶液呈酸性,则V1一定大于V2 |
| D、若反应后溶液呈碱性,则V1一定小于V2. |