题目内容
将Al片投入某无色澄清溶液中,产生大量H2,则该溶液中可能含有的微粒是( )
| A、K+、OH-、NO3-、Cl- |
| B、H+、Na+、CO32-、Cl- |
| C、H+、K+、NO3-、Cl- |
| D、Cu2+、H+、Cl-、SO42- |
考点:离子共存问题
专题:
分析:溶液无色透明,则不含有颜色的离子,如Cu2+、MnO4-等,放入铝片,立刻有大量H2生成,溶液可能为碱,也可能呈酸,加入铝能产生氢气,且离子之间不发生任何反应的离子能大量共存.
解答:
解:A.碱性条件下该组离子之间不反应,则离子之间能够大量共存,故A正确;
B.H+、CO32-反应生成二氧化碳和水,不能大量共存,故B错误;
C.溶液无色,在酸性条件下不能生成氢气,碱溶液中与H+反应,则不能大量共存,故C错误;
D.Cu2+有颜色,不符合题目无色的要求,故D错误.
故选 A.
B.H+、CO32-反应生成二氧化碳和水,不能大量共存,故B错误;
C.溶液无色,在酸性条件下不能生成氢气,碱溶液中与H+反应,则不能大量共存,故C错误;
D.Cu2+有颜色,不符合题目无色的要求,故D错误.
故选 A.
点评:本题考查离子的共存问题,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,熟悉离子反应发生的条件及离子之间的反应即可解答,难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
下列各组物质的分类正确的是( )
| 选项 | 电解质 | 纯净物 | 碱性氧化物 | 酸性氧化物 |
| A | 酒精溶液 | 冰水混合物 | CaO | SO2 |
| B | BaSO4 | 液氯 | Fe2O3 | CO2 |
| C | Fe(OH)3 | CuSO4?5H2O | Al2O3 | SO2 |
| D | NH3 | 水银 | CuO | NO2 |
| A、A | B、B | C、C | D、D |
下列原子的价电子排布图正确的是( )
A、 |
B、 |
C、 |
D、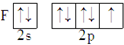 |
下列对Na2CO3与NaHCO3的描述正确的是( )
| A、Na2CO3比NaHCO3的溶度大 |
| B、受热时NaHCO3比Na2CO3稳定 |
| C、澄清的石灰水能与Na2CO3反应而不与NaHCO3反应 |
| D、向相同浓度的NaHCO3与Na2CO3溶液中分别滴入2滴酚酞溶液,前者红色更深 |
发射“天宫一号”使用的是“长征二号F”T1运载火箭,火箭的燃料是偏二甲肼(化学式为C2H8N2,其中C和N均为-2价),它与四氧化二氮一旦混合便会剧烈燃烧,产生大量气体并释放出大量的热,该反应的化学方程式为:2N2O4+C2H8N2=3N2+2CO2+4H2O,则下列说法正确的是( )
| A、该反应不属于氧化还原反应 |
| B、该反应中氧化剂是N2O4 |
| C、该反应中只有氮元素被氧化 |
| D、N2O4在反应过程中发生氧化反应 |
设NA为阿佛加德罗常数,下列叙述中不正确的是( )
| A、常温下,46 g 红棕色二氧化氮气体中含有N、O原子个数和为3NA |
| B、标准状况下,1 NA CH3Cl所占的体积约为22.4 L |
| C、N2(g)+3H2(g)?2NH3(g)△H=-a kJ/mol,现向一密闭容器中通入2 NA个氨气分子反应完全后,吸收a kJ热量 |
| D、足量铜与1 L 18mol?L-1浓硫酸反应可以得到SO2的分子总数小于9 NA |
如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
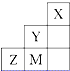

| A、电负性:Y>Z>M |
| B、离子半径:M->Z2->Y- |
| C、ZM2分子中各原子的最外层均满足8电子稳定结构 |
D、Z元素基态原子最外层电子排布图为 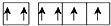 |
 甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是
甲烷水蒸气重整制合成气是利用甲烷资源的途径之一,该过程的主要反应是 Ⅰ.常温下ClO2是黄绿色,有刺激性气味的气体,液态呈红棕色,熔点为-59℃,沸点为11.0℃;
Ⅰ.常温下ClO2是黄绿色,有刺激性气味的气体,液态呈红棕色,熔点为-59℃,沸点为11.0℃;