题目内容
氧原子的最外层电子排布轨道表示式: ;列举2个能说明氧、硫两种元素非金属性强弱事实: .
考点:原子核外电子排布,非金属在元素周期表中的位置及其性质递变的规律
专题:
分析:氧原子最外层6个电子,其中2p轨道中还有4个电子;氢化物的稳定性越强,非金属越强;对应的单质的氧化性越强,则非金属性越强.
解答:
解:氧原子最外层6个电子,其中2s轨道还有2个电子,2p轨道还有4个电子,氧原子的最外层轨道表示式为: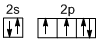 ;
;
水比硫化氢稳定,则氧的非金属性大于硫;氧可以置换硫化氢中的硫等,则氧的非金属性大于硫;
故答案为: ;水比硫化氢稳定,氧可以置换硫化氢中的硫等;
;水比硫化氢稳定,氧可以置换硫化氢中的硫等;
 ;
;水比硫化氢稳定,则氧的非金属性大于硫;氧可以置换硫化氢中的硫等,则氧的非金属性大于硫;
故答案为:
 ;水比硫化氢稳定,氧可以置换硫化氢中的硫等;
;水比硫化氢稳定,氧可以置换硫化氢中的硫等;
点评:本题考查轨道式的书写、元素周期律知识,侧重于学生的分析能力的考查,注意元素的性质与对应单质、化合物的性质的关系,注意把握非金属性强弱的比较规律,难度不大.

练习册系列答案
相关题目
已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
H2(g)+
O2(g)=H2O(g)△H2
C(s)+O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(l)△H1
H2(g)+
| 1 |
| 2 |
C(s)+O2(g)=CO2(g)△H3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
| A、12△H3+10△H2-2△H1 |
| B、2△H1-10△H2-12△H3 |
| C、12△H3-10△H2-2△H1 |
| D、△H1-10△H2-12△H3 |
下列原子的价电子排布图正确的是( )
A、 |
B、 |
C、 |
D、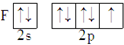 |
发射“天宫一号”使用的是“长征二号F”T1运载火箭,火箭的燃料是偏二甲肼(化学式为C2H8N2,其中C和N均为-2价),它与四氧化二氮一旦混合便会剧烈燃烧,产生大量气体并释放出大量的热,该反应的化学方程式为:2N2O4+C2H8N2=3N2+2CO2+4H2O,则下列说法正确的是( )
| A、该反应不属于氧化还原反应 |
| B、该反应中氧化剂是N2O4 |
| C、该反应中只有氮元素被氧化 |
| D、N2O4在反应过程中发生氧化反应 |
设NA为阿佛加德罗常数,下列叙述中不正确的是( )
| A、常温下,46 g 红棕色二氧化氮气体中含有N、O原子个数和为3NA |
| B、标准状况下,1 NA CH3Cl所占的体积约为22.4 L |
| C、N2(g)+3H2(g)?2NH3(g)△H=-a kJ/mol,现向一密闭容器中通入2 NA个氨气分子反应完全后,吸收a kJ热量 |
| D、足量铜与1 L 18mol?L-1浓硫酸反应可以得到SO2的分子总数小于9 NA |
单质硫在NaOH的热溶液中发生歧化反应:3S+6NaOH→2Na2S+Na2SO3+3H2O,若硫过量,进一步生成Na2Sx(x≤5)和Na2S2O3,将2.56g硫与含0.06molNaOH的热溶液充分反应恰好生成amolNa2S3和bmol Na2S2O3,再加入足量NaClO-NaOH的混合溶液,硫元素全部转化为Na2SO4,转移电子n mol,则以下正确的是( )
| A、a=2b |
| B、2a=b |
| C、n=0.48 |
| D、b=0.02 |
如图为元素周期表中短周期的一部分,关于Y、Z、M的说法正确的是( )
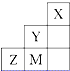

| A、电负性:Y>Z>M |
| B、离子半径:M->Z2->Y- |
| C、ZM2分子中各原子的最外层均满足8电子稳定结构 |
D、Z元素基态原子最外层电子排布图为 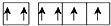 |
 室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol?L-1Ba(OH)2溶液时,生成的沉淀BaSO4和pH的变化关系如图所示(不考虑溶液混合时体积的变化).下列说法正确的是( )
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol?L-1Ba(OH)2溶液时,生成的沉淀BaSO4和pH的变化关系如图所示(不考虑溶液混合时体积的变化).下列说法正确的是( )| A、图中A点对应溶液的pH:a=1 |
| B、生成沉淀的最大值m=2.33g |
| C、原混合液中盐酸的浓度为0.1 mol?L-1 |
| D、当V[Ba(OH)2]=10 mL时,发生反应的离子方程式为:Ba2++SO42-→BaSO4↓ |