��Ŀ����
��֪��25��ʱ�����ᡢ̼���������ĵ���ƽ�ⳣ���ֱ�Ϊ��
���� Ka=1.75��10-5
̼�� Ka1=4.30��10-7 Ka2=5.61��10-11
������ Ka1=1.54��10-2 Ka2=1.02��10-7
��1��д��̼��ĵ�һ������ƽ�ⳣ������ʽ��Ka1= ��
̼��ĵڶ�������ȵ�1������ ������ס������ѡ�����ԭ���� ��
��2������ͬ�����£��ԱȽ�H2CO3��HCO3-��HSO3-������ǿ���� �� ��
��3���������¶Ȳ��䣬�ڴ�����Һ�м����������ᣬ���������С���� ������ţ�
A��c��CH3COO-�� B��c��H+�� C��
D������ĵ���ȣ�
���� Ka=1.75��10-5
̼�� Ka1=4.30��10-7 Ka2=5.61��10-11
������ Ka1=1.54��10-2 Ka2=1.02��10-7
��1��д��̼��ĵ�һ������ƽ�ⳣ������ʽ��Ka1=
̼��ĵڶ�������ȵ�1������
��2������ͬ�����£��ԱȽ�H2CO3��HCO3-��HSO3-������ǿ����
��3���������¶Ȳ��䣬�ڴ�����Һ�м����������ᣬ���������С����
A��c��CH3COO-�� B��c��H+�� C��
| c(H+)?c(CH3COO-) |
| c(CH3COOH) |
���㣺���������ˮ��Һ�еĵ���ƽ��
ר�⣺
��������1��̼��ĵ�һ�����뷽��ʽΪH2CO3?H++HCO3-������ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ�����ݵ���ƽ���ƶ�ԭ��������
��2������H2CO3��HCO3-��HSO3-�ĵ���ƽ�ⳣ��ȷ�����Ե�ǿ����
��3����������ᣬ����ĵ���ƽ�������ƶ�����c��CH3COO-����С������ĵ���̶ȼ�С�����¶Ȳ��䣬��������ƽ�ⳣ�����䣬������ʱc��H+������
��2������H2CO3��HCO3-��HSO3-�ĵ���ƽ�ⳣ��ȷ�����Ե�ǿ����
��3����������ᣬ����ĵ���ƽ�������ƶ�����c��CH3COO-����С������ĵ���̶ȼ�С�����¶Ȳ��䣬��������ƽ�ⳣ�����䣬������ʱc��H+������
���
�⣺��1��̼��ĵ�һ�����뷽��ʽΪH2CO3?H++HCO3-������ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ����K1=
��̼��ĵڶ����������ڵ�һ����������������ӶԵڶ������������ã����Աȵ�һ�����ѣ�
�ʴ�Ϊ��
�����ѣ���һ����������������ӶԵڶ������������ã�
��2��H2CO3��HCO3-��HSO3-�ĵ���ƽ�ⳣ���ֱ��ǣ�4.30��10-7��5.61��10-11��1.02��10-7����������˳���ǣ�H2CO3��HSO3-��HCO3-��
�ʴ�Ϊ��H2CO3��HSO3-��HCO3-��
��3����������ᣬ����ĵ���ƽ�������ƶ�����c��CH3COO-����С������ĵ���̶ȼ�С�����¶Ȳ��䣬��������ƽ�ⳣ�����䣬������ʱc��H+�����ʴ�Ϊ��AD��
| c(H +)c(HCO 3 -) |
| c(H 2CO 3) |
�ʴ�Ϊ��
| c(H +)c(HCO 3 -) |
| c(H 2CO 3) |
��2��H2CO3��HCO3-��HSO3-�ĵ���ƽ�ⳣ���ֱ��ǣ�4.30��10-7��5.61��10-11��1.02��10-7����������˳���ǣ�H2CO3��HSO3-��HCO3-��
�ʴ�Ϊ��H2CO3��HSO3-��HCO3-��
��3����������ᣬ����ĵ���ƽ�������ƶ�����c��CH3COO-����С������ĵ���̶ȼ�С�����¶Ȳ��䣬��������ƽ�ⳣ�����䣬������ʱc��H+�����ʴ�Ϊ��AD��
������������ѣ�����ѧ��Ӧ�õ���ƽ�ⳣ����ƽ���ƶ�����������⣬ע���˶����ݵķ�����Ӧ�ã��Ϻõ�ѵ��ѧ��������������������

��ϰ��ϵ�д�
 ���б�ˢ��ϵ�д�
���б�ˢ��ϵ�д�
�����Ŀ
����ͼʾ��Ӧ��װ���Լ���������ȷ���ǣ�������
A�� ���� |
B�� �Ƶ���ɫ��Ӧ |
C�� ���� |
D�� ���� |
��AlCl3��FeCl3�Ļ��Һ�У��ȼ��������KI��Һ���ټ���������Na2S��Һ�����õ��ij�������Ҫ�ǣ�������
| A��Fe2S3��I2��S |
| B��Al��OH��3��I2��S |
| C��Fe��OH��3��Al��OH��3��S |
| D��FeS��S��Al��OH��3 |
ijͬѧͨ��ϵͳʵ��̽�������仯��������ʣ�������ȷ���ܴﵽĿ���ǣ�������
| A���û���μӵķ����ɼ����Ȼ�����Һ������������Һ |
| B�����Ȼ�����Һ�еμӹ�����ˮ�����յõ�������Һ |
| C������������Ũ���ᷴӦ�Ƶô�����NO2 |
| D��AlCl3��Һ�������ɵõ���ˮ�Ȼ������� |
�ڷ�Ӧ3S+6KOH=K2SO3+2K2S+3H2O�У��������뱻��ԭ����ԭ����֮��Ϊ��������
| A��1��2 | B��2��1 |
| C��1��1 | D��3��2 |
ij���廯����A�����磬���ۻ�������ˮ������ȫ���룮���й�������A��˵���У���ȷ���ǣ�������
| A��AΪ�ǵ���� |
| B��AΪǿ����� |
| C��A�Ȳ��ǵ����Ҳ���Ƿǵ��� |
| D��A������� |
�������ӻ�ԭ�ӣ����ǡ�8���ӽṹ�����ǣ�������
| A��Na+ |
| B��Cl- |
| C��H+ |
| D��F- |
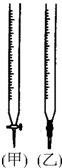 ijѧ����0.10mol/L��NaOH��Һ�ζ�ijŨ�ȵ����ᣮ��¼�������£�
ijѧ����0.10mol/L��NaOH��Һ�ζ�ijŨ�ȵ����ᣮ��¼�������£�