题目内容
13.实验室用下列装置从NaBr溶液中制备单质溴,其合理的是( )| A. | 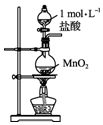 用装置甲制取氯气 | B. | 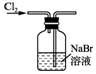 用装置乙氧化溴离子 | ||
| C. | 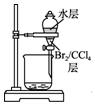 用装置丙分离出溴的CCl4溶液 | D. | 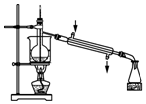 用装置丁获得单质溴 |
分析 A.1mol/L盐酸不是浓盐酸,与二氧化锰不反应;
B.导管应长进短出;
C.溴的CCl4溶液在下层,水在上层;
D.蒸馏时温度计测定馏分的温度,且冷却水下进上出.
解答 解:A.1mol/L盐酸不是浓盐酸,与二氧化锰不反应,应选浓盐酸、二氧化锰加热制备氯气,故A错误;
B.导管应长进短出,图中气体将溶液排出,故B错误;
C.溴的CCl4溶液在下层,水在上层,则图中分液装置可分离,故C正确;
D.蒸馏时温度计测定馏分的温度,且冷却水下进上出,图中温度计的位置、冷水方向不合理,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、气体的制备、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
1.2016年12月,中共中央、国务院印发了《关于全面推行河长制的意见》,进一步加强水污染治理工作.下列做法不应该提倡的是( )
| A. | 用碱性废水中和处理酸性废水 | |
| B. | 将工业废液排入海洋以减少河道污染 | |
| C. | 生活污水无害化处理后用于绿化灌溉 | |
| D. | 推广使用高效、低毒农药,减轻水体污染 |
8.常温下,取铝土矿(含有Al2O3、FeO、Fe2O3、SiO2等物质)用硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
| A. | 加入过量NaOH溶液:Na+、AlO2-、OH-、SO42- | |
| B. | 加入过量氨水:NH4+、Al3+、OH-、SO42- | |
| C. | 通入过量SO2:Fe2+、H+、SO32-、SO42- | |
| D. | 加入过量NaClO溶液:Fe2+、Na+、ClO-、SO42- |
5.从海带中提取碘应该包括灼烧、溶解、过滤、氧化、萃取、蒸馏等过程.下列有关图示操作正确的是( )
| A. | 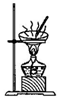 用装置甲将海带灼烧成灰 | B. | 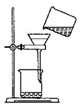 用装置乙过滤得含I-的溶液 | ||
| C. | 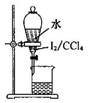 用装置丙分离出碘的CCl4溶液 | D. | 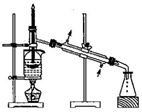 用装置丁蒸馏获得碘并回收CCl4 |
2.对反应A(s)+3B(g)?2C(g)+D(g)来说,下列反应速率最快的是( )
| A. | v(A)=0.02 mol/(L•s) | B. | v(B)=0.6 mol/(L•min) | ||
| C. | v(C)=0.5 mol/(L•min) | D. | v(D)=0.01 mol/(L•s) |
5.在学习中,我们经常应用类推法.下列表格左边正确,类推法应用于右边也正确的是( )
| A | 向FeCl2溶液中滴入氯水2Fe2++Cl2=2Fe3++2C l- | 向FeC l2溶液中滴入碘水2Fe2++I2=2Fe3++2I- |
| B | 向澄清石灰水中通入少量CO2 气体Ca2++2OH-+CO2=CaCO3↓+H2O | 向澄清石灰水中通入少量SO2 气体Ca2++2OH-+SO2=CaSO3↓+H2O |
| C | 向Na2CO3溶液中滴入稀HNO3CO32-+2H+=CO2↑+H2O | 向Na2SO3溶液中滴入稀HNO3SO32-+2H+=SO2↑+H2O |
| D | CO2 通入漂白粉溶液中CO2+Ca2++2ClO-+H2O=CaCO3↓+2HClO | SO2通入漂白粉溶液中SO2+Ca2++2ClO-+H2O=CaSO3↓+2HClO |
| A. | A | B. | B | C. | C | D. | D |
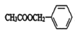 )存在于可可、咖啡、草莓等食品中,常用作食品香精.请回答下列问题:
)存在于可可、咖啡、草莓等食品中,常用作食品香精.请回答下列问题: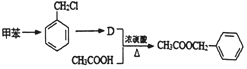
 的反应条件为光照
的反应条件为光照 生成D的反应化学方程式为
生成D的反应化学方程式为