题目内容
2.对反应A(s)+3B(g)?2C(g)+D(g)来说,下列反应速率最快的是( )| A. | v(A)=0.02 mol/(L•s) | B. | v(B)=0.6 mol/(L•min) | ||
| C. | v(C)=0.5 mol/(L•min) | D. | v(D)=0.01 mol/(L•s) |
分析 反应速率之比等于化学计量数之比,则反应速率与化学计量数的比值越大,反应速率越快,以此来解答.
解答 解:反应速率与化学计量数的比值越大,反应速率越快,则
A.A为固体,不能表示反应速率;
B.$\frac{0.6}{3}$=0.2;
C.$\frac{0.5}{2}$=0.25;
D.$\frac{0.01×60}{1}$=0.6,
显然D中比值最大,反应速率最快,
故选D.
点评 本题考查化学反应速率的比较,为高频考点,把握反应速率与化学计量数的关系为解答的关键,侧重分析与计算能力的考查,注意比值法应用及速率单位要统一,题目难度不大.

练习册系列答案
相关题目
13.实验室用下列装置从NaBr溶液中制备单质溴,其合理的是( )
| A. | 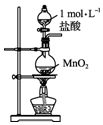 用装置甲制取氯气 | B. | 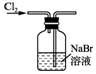 用装置乙氧化溴离子 | ||
| C. | 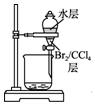 用装置丙分离出溴的CCl4溶液 | D. | 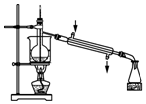 用装置丁获得单质溴 |
10.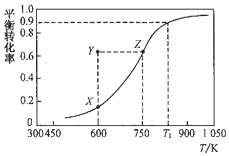 甲醇脱氢可制取甲醛:CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化的曲线如图所示(已知反应在IL 的密闭容器中进行).下列有关说法正确的是( )
甲醇脱氢可制取甲醛:CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化的曲线如图所示(已知反应在IL 的密闭容器中进行).下列有关说法正确的是( )
 甲醇脱氢可制取甲醛:CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化的曲线如图所示(已知反应在IL 的密闭容器中进行).下列有关说法正确的是( )
甲醇脱氢可制取甲醛:CH3OH(g)?HCHO(g)+H2(g),甲醇的平衡转化率随温度变化的曲线如图所示(已知反应在IL 的密闭容器中进行).下列有关说法正确的是( )| A. | 平衡常数:K600K>K750K | |
| B. | 从Y到Z点可通过增大压强实现 | |
| C. | 在Tl点K时,该反应的平衡常数为8.1 | |
| D. | 若工业上利用此反应进行生产,为了提高经济效益将反应温度升高至1050K以上 |
17.下列指定反应的离子方程式书写正确的是( )
| A. | 少量SO2 通入漂白粉溶液中:SO2+H2O+Ca2++3C1O-═CaSO4↓+2HC1O+Cl- | |
| B. | 石灰水与过量小苏打溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | FeCl2溶液中通入 C12:Fe2++Cl2═Fe3++2Cl- | |
| D. | NaAlO2 溶液中通入过量CO2:AlO2-+4CO2+2H2O═A13++4HCO3- |
7.已知电离常数的大小可以用来比较酸性的相对强弱,观察下表中的数据分析表格中两种弱酸可能涉及到的分子或离子,依据:较强酸+较弱酸盐=较弱酸+较强酸盐的反应规律,且较强酸和较弱酸盐按物质的量比为1:1发生反应,则最多可以写出的离子方程式的个数(不考虑难溶盐)是( )
| 弱酸 | 电离常数 | 弱酸 | 电离常数 |
| H2CO3 | Ka1=4.4×10-7 | H2C2O4 | Ka1=5.4×10-2 |
| Ka2=4.7×10-11 | Ka2=5.4×10-5 |
| A. | 2 | B. | 4 | C. | 6 | D. | 8 |
14.下列有关物质的俗称,正确的是( )
| A. | Fe2O3--铁红 | B. | SiO2--玛瑙 | C. | Na2SiO3水玻璃 | D. | NaHCO3--苏打 |
11.在实验室和生产生活中,安全是避免伤害和事故的保障.下列处理方法不正确的是( )
| A. | 金属钠着火时立即用沙子盖灭 | |
| B. | 制取有毒气体时需在通风橱中进行 | |
| C. | 将过期的化学药品直接倒入下水道 | |
| D. | 给试管中液体加热时试管口要避开人 |
14.分子式C8H8O2的有机物,其结构中含有苯环且可以与饱和NaHCO3溶液反应放出气体的同分异构体有(不考虑立体异构)( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |