题目内容
8.氧化还原反应在生活中普遍存在,下列事实中不涉及氧化还原反应的是( )| A. | 金属锈蚀 | B. | 烟花燃放 | C. | 食物腐败 | D. | 水垢形成 |
分析 不涉及氧化还原反应,说明该反应中没有电子转移,其特征是没有元素化合价升降,
A.金属生锈过程中,铁失去电子被氧化;
B.燃放烟花过程中存在C、S元素化合价变化;
C.食物的腐败是食物缓慢氧化变质的过程;
D.钟乳石的形成是碳酸钙和碳酸氢钙之间长期的化学变化过程.
解答 解:A.金属生锈过程铁的化合价发生变化,属于氧化还原反应,故A错误;
B.燃放烟花爆竹时,C、S等元素化合价发生变化,所以属于氧化还原反应,故B错误;
C.食物的腐败是食物缓慢氧化变质的过程,属于氧化还原反应,故C错误;
D.钟乳石形成的反应是:CO2+CaCO3+H2O=Ca(HCO3)2,Ca(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$CO2+CaCO3↓+H2O,均不属于氧化还原反应,故D正确;
故选D.
点评 本题考查氧化还原反应的综合知识,题目难度不大,熟悉物质的性质以及发生的反应过程是解题的关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
18.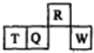 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | 含T的盐溶液一定能与碱反应 |
16.常温下,将pH值等于3的酸溶液和pH值等于11的Ba(OH)2溶液等体积混和,所得溶液的pH值( )
| A. | ≥7 | B. | ≤7 | C. | 一定等于7 | D. | 可能大于7 |
2. 石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )
石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )
 石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )
石墨晶体是层状结构,在每一层内,每个碳原子都跟其他3个碳原子相结合.据图分析,石墨晶体中碳原子数与共价键数之比为( )| A. | 3:2 | B. | 2:1 | C. | 1:3 | D. | 2:3 |
6.Ⅰ.某小组同学对一未知溶液进行了多次检测,其中三次检测结果如下表所示.
(1)三次检测结果中第三次检测结果肯定不正确.
Ⅱ.为了逐一除去溶液中SO42-和Mg2+并且最后所得溶液中不引入新的离子,该组同学选择适当试剂进行实验.可供选择的试剂有:稀HNO3、稀HCl、Ba(OH)2、Ba(NO3)2、NaOH、Na2CO3.相应的实验过程可用下图表示:
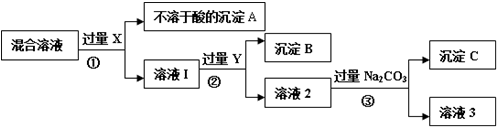
(2)写出实验流程中试剂X的化学式Ba(NO3)2.
(3)上述实验流程中加入过量Na2CO3的目的是使溶液中的Ba2+完全沉淀.
(4)按此实验方案得到的溶液3中肯定引入其他新的阴离子,可以向溶液3中加入适量的稀HNO3除去,写出其中一个反应的化学方程式2HNO3+Na2CO3═2NaNO3+H2O+CO2↑(或HNO3+NaOH=NaNO3+H2O).
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | MgSO4、NaNO3、KNO3、 |
| 第二次 | Mg (NO3)2、KNO3、Na2SO4 |
| 第三次 | Mg (NO3)2、Ba(NO3)2、Na2SO4 |
Ⅱ.为了逐一除去溶液中SO42-和Mg2+并且最后所得溶液中不引入新的离子,该组同学选择适当试剂进行实验.可供选择的试剂有:稀HNO3、稀HCl、Ba(OH)2、Ba(NO3)2、NaOH、Na2CO3.相应的实验过程可用下图表示:

(2)写出实验流程中试剂X的化学式Ba(NO3)2.
(3)上述实验流程中加入过量Na2CO3的目的是使溶液中的Ba2+完全沉淀.
(4)按此实验方案得到的溶液3中肯定引入其他新的阴离子,可以向溶液3中加入适量的稀HNO3除去,写出其中一个反应的化学方程式2HNO3+Na2CO3═2NaNO3+H2O+CO2↑(或HNO3+NaOH=NaNO3+H2O).
7.下列有关物质用途的说法错误的是( )
| A. | 乙烯作植物生长调节剂 | B. | 碳酸氢铵作化肥 | ||
| C. | 漂粉精作漂白剂 | D. | 生铁作航空材料 |

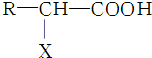 ,X的名称为氨基.
,X的名称为氨基. )易水解,其水解反应的产物为乙酸和
)易水解,其水解反应的产物为乙酸和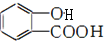 (填结构简式).
(填结构简式).