题目内容
18.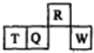 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | 含T的盐溶液一定能与碱反应 |
分析 由短周期元素R、T、Q、W的位置,可确定T、Q、W为第三周期的元素,R为第二周期元素,T所处的周期序数与族序数相等,则T为Al元素,故Q为Si元素,W为S元素,R为N元素,结合元素周期律与元素化合物性质解答.
解答 解:由短周期元素R、T、Q、W的位置,可确定T、Q、W为第三周期的元素,R为第二周期元素,T所处的周期序数与族序数相等,则T为Al元素,故Q为Si元素,W为S元素,R为N元素,
A.非金属性N>Si,其最简单气态氢化物的热稳定性:NH3>SiH4,故A正确;
B.非金属性Si<S,其最高价氧化物对应水化物的酸性强弱为:H2SiO3<H2SO4,故B正确;
C.同周期自左而右原子半径减小,同主族自上而下原子半径增大,则原子半径大小为:T>Q>R,故C正确;
D.T为Al,偏铝酸钠为含有铝的盐,但偏铝酸钠不与碱溶液反应,故D错误;
故选D.
点评 本题考查结构性质位置关系应用,题目难度不大,推断元素是解题关键,侧重对元素周期律的考查,明确原子结构与元素周期律、元素周期表的关系为解答关键.

练习册系列答案
相关题目
9.硅单质及其化合物应用范围很广.请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅.四氯甲硅烷(SiCl4)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

①写出由纯SiCl4制备高纯硅的化学反应方程式SiCl2+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl.
②整个制备过程必须严格控制无水无氧.SiCl4遇水剧烈反应生成H2SiO3和另一种物质,写出配平的化学反应方程式SiCl4+3H2O═H2SiO3↓+4HCl↑.
③为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需依次加入的试剂顺序是db.(填写字母代号)
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na2SO3溶液
(2)下列有头硅材料的说法不正确的是C(填字母).
A.碳化硅化学性质稳定、硬度大,可用于砂纸、砂轮的磨料
B.含4%硅的硅钢具有很高的导磁性,可用作变压器铁芯
C.硅橡胶保持良好的弹性,耐高温但不耐低温.
D.人造分子筛是一种硅酸盐,用作吸附剂和催化剂.
(3)硅酸钠水溶液俗称水玻璃,是一种防腐剂、防火剂和矿物胶.某同学为了证明Na2SiO3具有防火性能,做如下实验:取两个相同的小木条,分别放入蒸馏水和Na2SiO3饱和溶液中,使之充分吸湿、浸透,取出稍沥干(不再滴液)后,同时分别放置在酒精灯外焰处.观察到的现象如右表:设计实验①的目的是与实验②作对照,证明起防火作用的是Na2SiO3而不是水.
(1)制备硅半导体材料必须先得到高纯硅.四氯甲硅烷(SiCl4)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:

①写出由纯SiCl4制备高纯硅的化学反应方程式SiCl2+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl.
②整个制备过程必须严格控制无水无氧.SiCl4遇水剧烈反应生成H2SiO3和另一种物质,写出配平的化学反应方程式SiCl4+3H2O═H2SiO3↓+4HCl↑.
③为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需依次加入的试剂顺序是db.(填写字母代号)
a.碘水 b.氯水 c.NaOH溶液 d.KSCN溶液 e.Na2SO3溶液
(2)下列有头硅材料的说法不正确的是C(填字母).
A.碳化硅化学性质稳定、硬度大,可用于砂纸、砂轮的磨料
B.含4%硅的硅钢具有很高的导磁性,可用作变压器铁芯
C.硅橡胶保持良好的弹性,耐高温但不耐低温.
D.人造分子筛是一种硅酸盐,用作吸附剂和催化剂.
| 编号 | 实验 | 现象 |
| ① | 放入蒸馏水 | 木条燃烧 |
| ② | 放入Na2SiO3饱和溶液 | 木条不燃烧 |
6.小东发现野营篝火的火焰很小,便将木柴架空了一些,他这样做主要是为了( )
| A. | 方便添加木柴 | B. | 升高木柴的温度 | ||
| C. | 降低木柴的着火点 | D. | 使木柴与空气充分接触 |
13.将铁粉加入到一定量AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成为( )
| A. | 铁 | B. | 铁和铜 | C. | 铁和银 | D. | 铁、铜、银 |
7.下列关于化学用语叙述正确的是( )
| A. | H2O2的电子: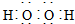 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | S2-离子的结构示意图: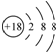 | |
| D. | FeSO4的电离方程式:FeSO4═Fe3++SO42- |
8.氧化还原反应在生活中普遍存在,下列事实中不涉及氧化还原反应的是( )
| A. | 金属锈蚀 | B. | 烟花燃放 | C. | 食物腐败 | D. | 水垢形成 |

 .
. .
.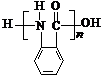 的单体.
的单体.
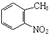 ,试剂a为酸性高锰酸钾溶液.
,试剂a为酸性高锰酸钾溶液.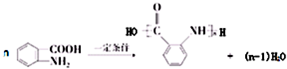 .
.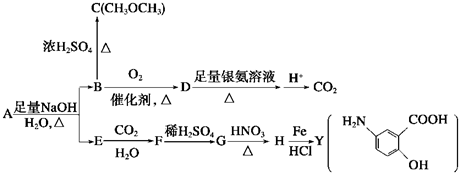
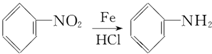
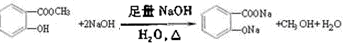 .
.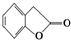 和
和 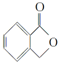 ,鉴别I和J的试剂为FeCl3或浓溴水.
,鉴别I和J的试剂为FeCl3或浓溴水.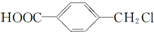 制得,写出K在浓硫酸作用下生成的聚合物的结构简式:
制得,写出K在浓硫酸作用下生成的聚合物的结构简式: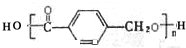 .
.