题目内容
参照反应Br2+H2→HBr+H的能量随反应历程变化的示意图,下列叙述中正确的是( )
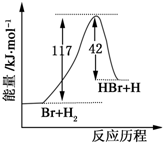

| A、反应物具有的总能量大于生成物具有的总能量 |
| B、正反应为吸热反应 |
| C、逆反应为吸热反应 |
| D、从图中可看出,该反应的反应热与反应途径有关 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:根据图象可知,反应物的总能量小于生成物的总能量,可知反应吸热,正反应为吸热反应则逆反应为放热反应,据此解答.
解答:
解:根据图象可知,反应物的总能量小于生成物的总能量,可知反应吸热,正反应为吸热反应则逆反应为放热反应,
A、从图上可知,反应物具有的总能量应该是小于生成物具有的总能量,故A错误;
B、根据图象可知,反应物的总能量小于生成物的总能量,可知反应吸热,故B正确;
C、根据图象可知,反应物的总能量小于生成物的总能量,可知反应吸热,正反应为吸热反应则逆反应为放热反应,故C错误;
D、从图中可以看出,反应热决定于反应物和生成物能量差,与反应途径无关,故D错误,
故选B.
A、从图上可知,反应物具有的总能量应该是小于生成物具有的总能量,故A错误;
B、根据图象可知,反应物的总能量小于生成物的总能量,可知反应吸热,故B正确;
C、根据图象可知,反应物的总能量小于生成物的总能量,可知反应吸热,正反应为吸热反应则逆反应为放热反应,故C错误;
D、从图中可以看出,反应热决定于反应物和生成物能量差,与反应途径无关,故D错误,
故选B.
点评:本题考查吸热反应的图象分析,注意正逆反应的焓变是相反数、焓变是反应物能量和与生成物能量和的差值,题目难度不大.

练习册系列答案
相关题目
用Pt电极放置于KOH溶液中,然后分别向两极通入CO和O2,即可产生电流,下列叙述中正确的是( )
①通入CO的电极为阴极
②通入CO的电极反应式为:2CO+O2+4e-═2CO2
③正极电极反应式为:O2+2H2O+4e-═4OH-
④负极电极反应式为:CO+4OH--2e-═CO32-+2H2O
⑤电池工作时溶液中的阳离子向原电池的负极移动
⑥放电时溶液中的阴离子向负极移动.
①通入CO的电极为阴极
②通入CO的电极反应式为:2CO+O2+4e-═2CO2
③正极电极反应式为:O2+2H2O+4e-═4OH-
④负极电极反应式为:CO+4OH--2e-═CO32-+2H2O
⑤电池工作时溶液中的阳离子向原电池的负极移动
⑥放电时溶液中的阴离子向负极移动.
| A、①④⑥ | B、③④⑥ |
| C、④⑤⑥ | D、①②③ |
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列说法正确的( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列说法正确的( )| A、此有机物含有如下的官能团:含有碳碳双键、羟基、羰基、羧基 |
| B、1mol该有机物与NaOH 溶液反应,耗2mol.与氢气反应耗氢气5mol |
| C、该有机分子中没有一个有手性碳 |
| D、该有机物不存在顺反异构 |
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
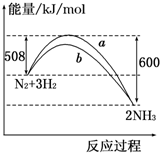

| A、该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ/mol |
| B、a曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热改变 |
| D、在温度、体积一定的条件下,若通入2 mol N2和6 mol H2反应后放出的热量为Q kJ,则184>Q |
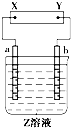 图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味气体放出,电解一段时间后,再加入相应的物质,溶液能与原来溶液完全一样.符合这一情况的是下表中的( )
图中X、Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味气体放出,电解一段时间后,再加入相应的物质,溶液能与原来溶液完全一样.符合这一情况的是下表中的( ) (1)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示.
(1)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示.