题目内容
四种短周期元素W、X、Y、Z 的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子核的质子数之比为1:2,X和Y的电子数之差为4.下列说法正确的是( )
| A、原子半径大小:Z>Y>X>W |
| B、由W元素形成的单质一定是原子晶体,其熔沸点很高 |
| C、W、Y、Z三种元素形成的气态氢化物中最稳定的是Z的气态氢化物 |
| D、Y、Z所形成的氧化物的水化物的酸性为:Y<Z |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:根据四种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子核质子数之比为1:2,X和Y的电子数之差为4,可知,W的原子序数为7时,此时推断出Y的原子序为18,所以W的原子序数为不超过7,可以按下列情况按序讨论:
①若W是H元素,则X是He元素、Y是C元素,其原子的最外层电子数之和为19,则Z最外层电子数是12,不存在这样的元素,故舍去;
②若W是He元素,则X是Be元素、Y是O元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
③若W是Li元素,则X是C元素、Y是Ne元素,其原子的最外层电子数之和为19,则Z最外层电子数是6,且Z原子序数大于Z,所以Z为S元素,符合题意;
④若W是Be元素,则X是O元素、Y是Mg元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
⑤若W是B元素,则X是Ne元素、Y是Si元素,其原子的最外层电子数之和为19,则Z最外层电子数是4,为Si元素,Y和Z不能是同一元素,故舍去;
⑥若W是C元素,则X是Mg元素、Y是S元素,其原子的最外层电子数之和为19,则Z最外层电子数是7,为Cl元素,符合题意;
⑦若W是N元素,则X是Si元素、Y是Ar元素,Z为短周期元素,所以没有符合条件的元素,故舍去;
所以存在的可能是③⑥,据此答题;
①若W是H元素,则X是He元素、Y是C元素,其原子的最外层电子数之和为19,则Z最外层电子数是12,不存在这样的元素,故舍去;
②若W是He元素,则X是Be元素、Y是O元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
③若W是Li元素,则X是C元素、Y是Ne元素,其原子的最外层电子数之和为19,则Z最外层电子数是6,且Z原子序数大于Z,所以Z为S元素,符合题意;
④若W是Be元素,则X是O元素、Y是Mg元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
⑤若W是B元素,则X是Ne元素、Y是Si元素,其原子的最外层电子数之和为19,则Z最外层电子数是4,为Si元素,Y和Z不能是同一元素,故舍去;
⑥若W是C元素,则X是Mg元素、Y是S元素,其原子的最外层电子数之和为19,则Z最外层电子数是7,为Cl元素,符合题意;
⑦若W是N元素,则X是Si元素、Y是Ar元素,Z为短周期元素,所以没有符合条件的元素,故舍去;
所以存在的可能是③⑥,据此答题;
解答:
解:根据四种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子核质子数之比为1:2,X和Y的电子数之差为4,可知,W的原子序数为7时,此时推断出Y的原子序为18,所以W的原子序数为不超过7,可以按下列情况按序讨论:
①若W是H元素,则X是He元素、Y是C元素,其原子的最外层电子数之和为19,则Z最外层电子数是12,不存在这样的元素,故舍去;
②若W是He元素,则X是Be元素、Y是O元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
③若W是Li元素,则X是C元素、Y是Ne元素,其原子的最外层电子数之和为19,则Z最外层电子数是6,且Z原子序数大于Z,所以Z为S元素,符合题意;
④若W是Be元素,则X是O元素、Y是Mg元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
⑤若W是B元素,则X是Ne元素、Y是Si元素,其原子的最外层电子数之和为19,则Z最外层电子数是4,为Si元素,Y和Z不能是同一元素,故舍去;
⑥若W是C元素,则X是Mg元素、Y是S元素,其原子的最外层电子数之和为19,则Z最外层电子数是7,为Cl元素,符合题意;
⑦若W是N元素,则X是Si元素、Y是Ar元素,Z为短周期元素,所以没有符合条件的元素,故舍去;
所以存在的可能是③⑥,
A.若为⑥,其原子半径大小顺序是X>Y>Z>W,故A错误;
B.若W是Li,则锂为金属晶体,故B错误;
C.W能形成氢化物,则W是C元素,Y是S元素、Z是Cl元素,元素的非金属性越强,其气态氢化物越稳定,这几种元素中非金属性最弱的是C元素,所以其气态氢化物最不稳定,故C正确;
D.Y、Z所形成的氧化物的水化物的酸性不一定是Y<Z,如H2SO4>HClO,故D错误;
故选C.
①若W是H元素,则X是He元素、Y是C元素,其原子的最外层电子数之和为19,则Z最外层电子数是12,不存在这样的元素,故舍去;
②若W是He元素,则X是Be元素、Y是O元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
③若W是Li元素,则X是C元素、Y是Ne元素,其原子的最外层电子数之和为19,则Z最外层电子数是6,且Z原子序数大于Z,所以Z为S元素,符合题意;
④若W是Be元素,则X是O元素、Y是Mg元素,其原子的最外层电子数之和为19,则Z最外层电子数是9,不存在这样的元素,故舍去;
⑤若W是B元素,则X是Ne元素、Y是Si元素,其原子的最外层电子数之和为19,则Z最外层电子数是4,为Si元素,Y和Z不能是同一元素,故舍去;
⑥若W是C元素,则X是Mg元素、Y是S元素,其原子的最外层电子数之和为19,则Z最外层电子数是7,为Cl元素,符合题意;
⑦若W是N元素,则X是Si元素、Y是Ar元素,Z为短周期元素,所以没有符合条件的元素,故舍去;
所以存在的可能是③⑥,
A.若为⑥,其原子半径大小顺序是X>Y>Z>W,故A错误;
B.若W是Li,则锂为金属晶体,故B错误;
C.W能形成氢化物,则W是C元素,Y是S元素、Z是Cl元素,元素的非金属性越强,其气态氢化物越稳定,这几种元素中非金属性最弱的是C元素,所以其气态氢化物最不稳定,故C正确;
D.Y、Z所形成的氧化物的水化物的酸性不一定是Y<Z,如H2SO4>HClO,故D错误;
故选C.
点评:本题主要考查了原子结构和元素周期律、晶体的类型等知识点,利用讨论法确定元素,再结合元素周期律解答,中等难度,解题时注意仔细审题.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去).关于混合粉末的组成判断正确的是( )
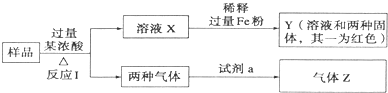

| A、一定含CuO和C |
| B、一定含Fe2O3、CuO和C |
| C、一定含CuO和C,一定不含Al |
| D、不管试剂a为H2O或饱和NaHCO3溶液,气体Z都为纯净物 |
 0.100 0mol/L的KOH标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
0.100 0mol/L的KOH标准溶液滴定未知浓度盐酸,其操作可分解为如下几步:
 )和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
)和C.经元素分析及相对分子质量测定,确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.


