题目内容
4.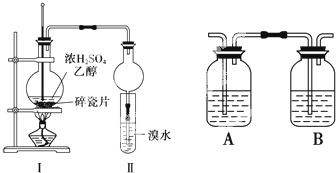 某化学兴趣小组用如图所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.
某化学兴趣小组用如图所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.(1)写出该实验中生成乙烯的化学方程式:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是BC
A、乙烯与溴水易发生取代反应?
B、使溴水褪色的反应,未必是加成反应?
C、使溴水褪色的物质,未必是乙烯?
(3)乙同学经过细致观察后认为试管中另一现象可证明反应中有乙烯生成,这个现象是试管底层有油状物质生成
(4)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加右上图装置,则A中的试剂应为氢氧化钠溶液; B中的试剂为品红,其作用是检验SO2是否除尽.
分析 (1)实验室制备乙烯所用的原料为乙醇,浓硫酸作催化剂、脱水剂,反应条件是加热到170℃;
(2)浓H2SO4具有强氧化性,能将乙醇氧化成碳,根据SO2具有还原性,也能与溴水反应使溴水褪色,据此即可解答;
(3)溴水中的溴与乙烯发生加成反应;
(4)在Ⅰ和Ⅱ之间增加图2装置,A装置是为了除去SO2和CO2,B装置是为了检验SO2是否除尽.
解答 解:(1)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,CH3CH2OH$→_{170℃}^{浓硫酸}$ CH2=CH2↑+H2O;
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$ CH2=CH2↑+H2O;
(2)浓H2SO4具有强氧化性,将乙醇氧化成碳,并且可以进一步反应,C+2H2SO4 $\frac{\underline{\;加热\;}}{\;}$CO2↑+2SO2↑+2H2O,SO2具有还原性,可以与Br2反应,SO2+Br2+2H2O=2HBr+H2SO4,所以BC正确,
故答案为:BC;
(3)溴水中的溴与乙烯发生加成反应,即CH2=CH2+Br2→CH2BrCH2Br,1,2-二溴乙烷在试管底层为油状物质,
故答案为:试管底层有油状物质生成;
(4)A装置是为了除去SO2,可用NaOH溶液,B装置是为了检验SO2是否除尽,可用品红溶液,
故答案为:氢氧化钠溶液;品红;检验SO2是否除尽.
点评 本题考查了实验室制取乙烯实验,明确实验原理是解本题关键,根据浓硫酸、乙烯的性质来分析解答,注意二氧化硫、乙烯都能使溴水褪色,但褪色原理不同,乙烯使溴水褪色是发生了加成反应,二氧化硫使溴水褪色是发生了氧化还原反应.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.已知铯(Cs)位于元素周期表中第七周期,ⅠA族.试判断下列对于铯的性质的预测中,正确的是( )
| A. | 它只有一种氧化物Cs2O | B. | 它与水剧烈反应 | ||
| C. | Cs+具有很强的氧化性 | D. | CsHCO3受热不易分解 |
15.已知pH=1的某溶液中存在较多的Ba2+、NO3-,则该溶液中还可能大量存在的离子组是( )
| A. | Fe3+、F-、Cl- | B. | Mg2+、SO42-、Br- | C. | Mg2+、Cl-、Fe2+ | D. | Na+、NH4+、Cu2+ |
13.下列说法不正确的是( )
| A. | 明矾和漂白粉均可用于自来水的杀菌、消毒 | |
| B. | 新制的0.1mol/L氯水中加入少量的CaCO3固体,HClO的物质的量浓度减小 | |
| C. | Na2O和Na2O2都能与H2O反应,其反应原理不相同 | |
| D. | O3、H2O2、SO2、Na2O2均有漂白性,其原理不尽相同 |
14.据权威刊物报道,1996年科学家在宇宙中发现H3分子.甲、乙、丙、丁四位学生对此报道的认识正确的是( )
| A. | 甲认为上述发现绝对不可能,因为H3分子违背了共价键理论 | |
| B. | 丁认为如果上述的发现存在,则证明传统的价键理论并不完善 | |
| C. | 丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+ | |
| D. | 乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体 |
 某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如图装置分别加热了NaNO3、Cu(NO3)2、AgNO3.(加热及夹持装置未画出)
某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如图装置分别加热了NaNO3、Cu(NO3)2、AgNO3.(加热及夹持装置未画出) 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.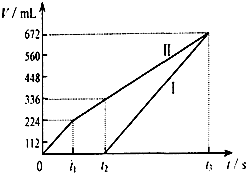 电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题.
电解200mL一定浓度的NaCl与CuSO4混合溶液,理论上两极所得气体的体积随时间变化的关系如下图所示(气体体积已换算成标准状况下的体积),根据图中信息回答下列问题.