题目内容
13.下列说法不正确的是( )| A. | 明矾和漂白粉均可用于自来水的杀菌、消毒 | |
| B. | 新制的0.1mol/L氯水中加入少量的CaCO3固体,HClO的物质的量浓度减小 | |
| C. | Na2O和Na2O2都能与H2O反应,其反应原理不相同 | |
| D. | O3、H2O2、SO2、Na2O2均有漂白性,其原理不尽相同 |
分析 A、明矾水溶液中铝离子水解生成氢氧化铝胶体,吸附悬浮杂质,净水作用,次氯酸钙有强氧化性的物质具有杀菌消毒的作用;
B、加入碳酸钙和氯水中盐酸反应促进化学平衡正向进行,次氯酸浓度增大;
C、氧化钠和水反应生成氢氧化钠,过氧化钠和水反应生成氢氧化钠和氧气;
D、O3、H2O2、Na2O2均有漂白性是氧化性的体现,SO2的漂白性不是氧化性.
解答 解:A、明矾溶液水电离产生的铝离子水解生成的氢氧化铝具有吸附性,能净水,但是明矾不具有强的氧化性所以不能杀菌消毒,漂白粉有效成分为次氯酸钙,次氯酸钙有强氧化性,可以杀菌消毒,故A错误;
B、氯水中存在化学平衡Cl2+H2O?HCl+HClO,加入少量的CaCO3固体,和盐酸反应促进平衡正向进行,次氯酸酸性小于碳酸,不与碳酸钙发生反应,HClO的物质的量浓度增大,故B错误;
C、氧化钠和水反应生成氢氧化钠,属于非氧化还原反应,过氧化钠和水反应生成氢氧化钠和氧气是氧化还原反应,二者反应原理不同,故C正确;
D、O3、H2O2、Na2O2均有漂白性是氧化性的体现,能氧化有机色素为无色,SO2的漂白性不是氧化性,是二氧化硫和有色物质结合生成不稳定的无色物质,加热恢复颜色,原理不同,故D正确;
故选AB.
点评 本题考查了物质性质的理解应用,主要是盐类水解,化学平衡影响因素分析,物质漂白性的原理分析,掌握基础是关键,题目难度中等.

练习册系列答案
 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
3. 醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:
醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:
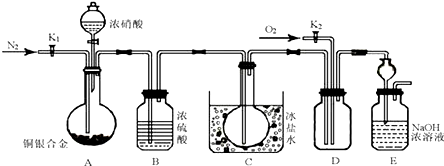
在化学工业上常用重铬酸钠的酸性溶液替代银和氧气,其模拟装置如图:
(B中为足量的重铬酸钠的酸性溶液,A中装有适量的1-丁醇和少量沸石,反应温度为93℃左右,E中为馏出物)
回答下列问题:
(1)上述装置图中,B仪器的名称是滴液漏斗,其使用前必须进行的操作是检漏.
(2)D仪器的名称是直形冷凝管,冷水应从b处进入(填a或b).
(3)实验操作过程中,若加热后发现未加沸石,则采取的正确方法是冷却后补加.
(4)将正丁醛粗产品提纯,要先进行操作Ⅰ,再进行操作Ⅱ,则操作Ⅰ是分液(填操作名称).
(5)反应温度应保持在93℃左右,其原因是既可保证正丁醛要及时蒸出,又可避免其被进一步氧化.
(6)上述装置图中,对应温度计C1、C2的放置判断正确的是c.
a.C1、C2均错误 b.C1错误C2正确 c.C1、C2均正确 d.C1正确C2错误
(7)正丁醛与新制的Cu(OH)2发生反应,该反应的化学方程式为CH3CH2CH2CHO+NaOH+2Cu(OH)2$\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O.
 醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:
醇的化学性质主要由羧基官能团所决定,如1-丁醇在银催化的条件下能与氧气反应生成正丁醛.相应醇和醛的有关物理性质如表:| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 1-丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
(B中为足量的重铬酸钠的酸性溶液,A中装有适量的1-丁醇和少量沸石,反应温度为93℃左右,E中为馏出物)
回答下列问题:
(1)上述装置图中,B仪器的名称是滴液漏斗,其使用前必须进行的操作是检漏.
(2)D仪器的名称是直形冷凝管,冷水应从b处进入(填a或b).
(3)实验操作过程中,若加热后发现未加沸石,则采取的正确方法是冷却后补加.
(4)将正丁醛粗产品提纯,要先进行操作Ⅰ,再进行操作Ⅱ,则操作Ⅰ是分液(填操作名称).
(5)反应温度应保持在93℃左右,其原因是既可保证正丁醛要及时蒸出,又可避免其被进一步氧化.
(6)上述装置图中,对应温度计C1、C2的放置判断正确的是c.
a.C1、C2均错误 b.C1错误C2正确 c.C1、C2均正确 d.C1正确C2错误
(7)正丁醛与新制的Cu(OH)2发生反应,该反应的化学方程式为CH3CH2CH2CHO+NaOH+2Cu(OH)2$\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O.
8.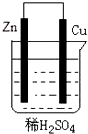 关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )
关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )
 关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )
关于如图所示装置的叙述:①Zn为正极,Cu为负极;②溶液中氢离子向负极移动;③电子从锌片经导线流向铜片;④铜极上有氢气产生;⑤若有0.1mol电子流过导线时,锌片质量减轻6.5g;⑥若有1mol电子流过导线,则产生的氢气为0.5mol.正确的是( )| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ③④⑥ |
2.将20克NaOH溶于水中,配制成1L溶液,则该溶液的物质的量浓度为( )
(已知NaOH的摩尔质量为40g/mol)
(已知NaOH的摩尔质量为40g/mol)
| A. | 0.1mol/L | B. | 0.5mol/L | C. | 4mol/L | D. | 1mol/L |
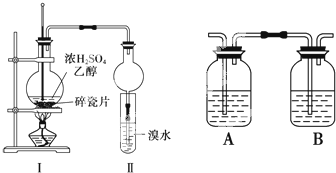 某化学兴趣小组用如图所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.
某化学兴趣小组用如图所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.