题目内容
将标准状况下的a升氨气溶于1000克水中,得到的氨水的密度为b克/毫升,则该氨水的物质的量的浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:计算题
分析:先计算出标况下aL氨气的物质的量,然后根据m=nM计算出氨气的质量,从而得出氨水溶液的质量,再计算出氨水的质量分数,最后根据c=
计算出该氨水的物质的量的浓度.
| 1000ρω |
| M |
解答:
解:标准状况下aL氨气的物质的量为:n=
=
mol,氨气的质量为:17g/mol×
mol=
g,
该氨水溶液的质量为:1000g+
g,
该氨水中溶质的质量分数为:ω=
=
,
该氨水的物质的量浓度为:c=
mol/L=
mol/L,
故选D.
| aL |
| 22.4L/mol |
| a |
| 22.4 |
| a |
| 22.4 |
| 17a |
| 22.4 |
该氨水溶液的质量为:1000g+
| 17a |
| 22.4 |
该氨水中溶质的质量分数为:ω=
| ||
1000g+
|
| 17a |
| 22400+17a |
该氨水的物质的量浓度为:c=
1000×b×
| ||
| 17 |
| 1000ab |
| 22400+17a |
故选D.
点评:本题考查了物质的量浓度计算,题目难度中等,注意掌握物质的量浓度的概念及计算方法,明确氨水溶液的体积不能用水和氨气的体积之和,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知室温时,0.1mol?L-1某一元酸HA的电离平衡常数约为1×10-7,下列叙述错误的是( )
| A、该溶液的pH=4 |
| B、此溶液中,HA约有0.1%发生电离 |
| C、加水稀释,HA的电离平衡向右移动,HA的电离平衡常数增大 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的106倍 |
下列叙述正确的是( )
| A、物质的量浓度为0.5 mol/L的MgCl2溶液,含有Cl- 个数为NA |
| B、V mL硫酸铁溶液中含有mg SO42-,则Fe3+的物质的量浓度为6.94m/V mol?L-1 |
| C、将58.5 g NaCl溶解于1 L水中配成溶液,所得溶液的物质的量浓度为1 mol?L-1 |
| D、用36.5%的浓盐酸(密度为1.25g?cm-3)配制成浓度为0.1mol?L-1的稀盐酸240ml,所需浓盐酸的体积为1.9mL |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、11.2L氧气所含的原子数为NA |
| B、1.9g的H3O+离子中含有的电子数为11NA |
| C、常温常压下96g NO2与N2O4的混合物含有的氧原子数为2NA |
| D、0.5mol/LH2SO4中的H+数为NA |
下列变化过程,属于吸热反应的是( )
(1)液氨汽化 (2)将胆矾加热变为白色粉末 (3)浓硫酸稀释 (4)氨催化氧化生成一氧化氮 (5)酸碱中和生成水 (6)NH4Cl与Ba(OH)2.8H2O.
(1)液氨汽化 (2)将胆矾加热变为白色粉末 (3)浓硫酸稀释 (4)氨催化氧化生成一氧化氮 (5)酸碱中和生成水 (6)NH4Cl与Ba(OH)2.8H2O.
| A、(1)(2)(6) |
| B、(1)(2)(4)(6) |
| C、(2)(6) |
| D、(2)(4)(6) |
下列说法正确的是( )
| A、宏观物体对外不显电性,是因为它们的组成微粒都是电中性的原子或分子 |
| B、利用化学方法,我们可以制造出新的分子,但不能制造出新的原子 |
| C、“低碳经济”就是要提倡大量使用煤、石油、天然气等化石燃料 |
| D、“绿色化学”的核心是利用化学原理对环境污染进行治理 |
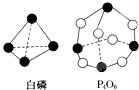 化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:E(P-P)=198kJ?mol-1、E(P-O)=360kJ?mol-1、E(O=O)=498kJ?mol-1,则反应P4(白磷)燃烧生成P4O6的热化学方程式为
化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:E(P-P)=198kJ?mol-1、E(P-O)=360kJ?mol-1、E(O=O)=498kJ?mol-1,则反应P4(白磷)燃烧生成P4O6的热化学方程式为