题目内容
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、11.2L氧气所含的原子数为NA |
| B、1.9g的H3O+离子中含有的电子数为11NA |
| C、常温常压下96g NO2与N2O4的混合物含有的氧原子数为2NA |
| D、0.5mol/LH2SO4中的H+数为NA |
考点:阿伏加德罗常数
专题:
分析:A、氧气所处的状态不明确;
B、依据n=
计算物质的量,结合微粒计算质子数;
C、根据NO2与N2O4的最简式均为NO2来分析;
D、溶液体积不明确.
B、依据n=
| m |
| M |
C、根据NO2与N2O4的最简式均为NO2来分析;
D、溶液体积不明确.
解答:
解:A、氧气所处的状态不明确,故11.2L氧气的物质的量不明确,故A错误;
B、1.9gH3O+离子的物质的量n=
=0.1mol,而1molH3O+离子含11mol质子,故0.1molH3O+离子含1.1mol质子,故B正确;
C、NO2与N2O4的最简式均为NO2,故96gNO2与N2O4中含有NO2的物质的量为2mol,故含有的氧原子的物质的量为4mol,故C错误;
D、溶液体积不明确,故无法计算H+数,故D错误.
故选B.
B、1.9gH3O+离子的物质的量n=
| m |
| M |
C、NO2与N2O4的最简式均为NO2,故96gNO2与N2O4中含有NO2的物质的量为2mol,故含有的氧原子的物质的量为4mol,故C错误;
D、溶液体积不明确,故无法计算H+数,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
反应N2(g)+O2(g)?2NO(g)在恒容密闭容器中进行,达到平衡后,充入N2,下列说法正确的是( )
| A、平衡向逆反应方向移动,N2和O2的转化率都减小 |
| B、平衡向正反应方向移动,N2和O2的转化率都增大 |
| C、压强增大平衡不移动,N2的转化率不变 |
| D、平衡向正反应方向移动,N2的转化率减小,O2的转化率增大 |
下列各装置中,不能构成原电池的是(电解质都为稀硫酸)( )
A、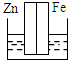 |
B、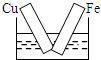 |
C、 |
D、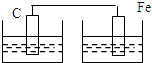 |
热化学方程式C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ/mol表示( )
| A、碳和水反应吸收131.3kJ能量 |
| B、1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量 |
| C、1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ |
| D、1个固态碳原子和1个水蒸气分子反应吸热131.1kJ |
将标准状况下的a升氨气溶于1000克水中,得到的氨水的密度为b克/毫升,则该氨水的物质的量的浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
设NA为阿伏加德罗常数,下列说法中,正确的是( )
| A、2L1mol/LNa2SO4溶液中含有的离子总数为3NA |
| B、16 g CH4所含原子数目为NA |
| C、18g NH4+ 所含电子数目为11NA |
| D、18 g水所含分子数目为NA |
下列物质中,摩尔质量最大的是 ( )
| A、10mL H2O |
| B、0.1mol HCl |
| C、24g Mg |
| D、1g CaCO3 |
下列离子方程式正确的是( )
| A、氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++2OH-+2 HCO3-=CaCO3↓+CO32-+2H2O |
| C、向CuSO4溶液中加入Ba(OH)2溶液,观察到有蓝色沉淀生成:Cu2++2OH-=Cu(OH)2↓ |
| D、FeSO4溶液中加H2O2溶液:Fe2++2H2O2+4H+=Fe3++4H2O |