题目内容
16.NA代表阿伏加德罗常数的值,下列说法正确的是( )| A. | 16gO2分子数为NA | |
| B. | 在常温常压下,22.4L氖气含有的原子数为NA | |
| C. | 1mol H2O在标准状况下所占有的体积约为22.4L | |
| D. | 1mol H2O2完全分解时,转移的电子总数为NA |
分析 A.计算物质的量n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$;
B.标准状况下气体摩尔体积为22.4L/mol;
C.标准状况下水不是气体;
D.过氧化氢分解生成水和氧气,氧元素化合价-1价变化为-2价和0价.
解答 解:A.16gO2物质的量=$\frac{16g}{32g/mol}$=0.5mol,分子数为0.5NA,故A错误;
B.在常温常压下,22.4L氖气物质的量不是1mol,故B错误;
C.标准状况下水不是气体,所占有的体积不是22.4L,故C错误;
D.2H2O2=2H2O+O2,2mol过氧化氢分解电子转移为2mol,1mol H2O2完全分解时,转移的电子总数为NA,故D正确;
故选D.
点评 本题考查了物质的量和阿伏伽德罗常数的有关计算,题目难度不大,应注意氧化还原反应、气体摩尔体积条件应用和公式的运用.

练习册系列答案
相关题目
17.中国科学院成功开发出一种新型铝-石墨双离子电池,大幅提升了电池的能量密度.该电池充电时的总反应为:Al+xC+Li++PF6-═AlLi+CxPF6,有关该电池说法正确的是( )
| A. | 放电时,电子由石墨沿导线流向铝 | |
| B. | 放电时,正极反应式为:Al+Li++e-═AlLi | |
| C. | 充电时,铝电极质量增加 | |
| D. | 充电时,PF6-向阴极移动 |
7.短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的简单气态氢化物的水溶液呈碱性,乙位于第ⅤA族,甲和丙同主族,丁的最外层电子数和电子层数相等,下列说法正确的是( )
| A. | 金属性:丙>甲 | |
| B. | 原子半径:r(丁)>r(丙)>r(乙)>r(甲) | |
| C. | 乙、丙、丁的简单离子的电子层结构相同 | |
| D. | 甲和乙以1:4形成的简单阳离子含11个电子 |
4.有机物甲、乙的结构如图所示,下列说法错误的是( )
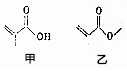

| A. | 甲、乙互为同分异构体 | |
| B. | 甲、乙都能发生取代、加成和水解反应 | |
| C. | 甲、乙都能使酸性的高锰酸钾褪色 | |
| D. | 等物质的量的甲和乙与足量的NaOH溶液反应,消耗NaOH的物质的量相等 |
11.下列说法不正确的是( )
| A. | HBr比HCl的还原性强 | |
| B. | 卤素是非金属性较强的元素,故其单质只有氧化性 | |
| C. | 碘难溶于水,易溶于有机溶剂 | |
| D. | 碘单质能使湿润的碘化钾淀粉试纸变蓝 |
1.已知:CH3CH2CH2CH3(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2878kJ•mol-1
(CH3)2CHCH3(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ•mol-1.
下列说法正确的是( )
(CH3)2CHCH3(g)+$\frac{13}{2}$O2(g)=4CO2(g)+5H2O(l)△H=-2869kJ•mol-1.
下列说法正确的是( )
| A. | 正丁烷分子储存的能量小于异丁烷 | |
| B. | 正丁烷的稳定性大于异丁烷 | |
| C. | 异丁烷转化为正丁烷的过程是一个放热过程 | |
| D. | 异丁烷转化为正丁烷的过程是一个吸热过程 |
6.下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | Na2S有强还原性 | 用于除去废水中的Cu2+和Hg2+ |
| B | CaCO3是难溶物 | CaCl2溶液中通入CO2产生白色沉淀 |
| C | Zn具有还原性和导电性 | 可用作锌锰干电池的负极材料 |
| D | 浓H2SO4有强氧化性 | 浓H2SO4可用于干燥SO2 |
| A. | A | B. | B | C. | C | D. | D |


 、K
、K .
. .(本题不考虑
.(本题不考虑 结构).
结构).