题目内容
4.有机物甲、乙的结构如图所示,下列说法错误的是( )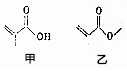
| A. | 甲、乙互为同分异构体 | |
| B. | 甲、乙都能发生取代、加成和水解反应 | |
| C. | 甲、乙都能使酸性的高锰酸钾褪色 | |
| D. | 等物质的量的甲和乙与足量的NaOH溶液反应,消耗NaOH的物质的量相等 |
分析 A.甲为CH3C(COOH)=CH2、乙为CH2=CHCOOCH3,分子式相同,结构不同;
B.均含碳碳双键,甲中含-COOH,乙中含-COOC-;
C.均含碳碳双键;
D.-COOH、-COOC-均与NaOH以1:1反应.
解答 解:A.甲为CH3C(COOH)=CH2、乙为CH2=CHCOOCH3,分子式相同,结构不同,二者互为同分异构体,故A正确;
B.均含碳碳双键,甲中含-COOH,乙中含-COOC-,均可发生加成、取代反应,但甲不能发生水解反应,故B错误;
C.均含碳碳双键,都能使酸性的高锰酸钾褪色,故C正确;
D.-COOH、-COOC-均与NaOH以1:1反应,则等物质的量的甲和乙与足量的NaOH溶液反应,消耗NaOH的物质的量相等,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意烯烃、羧酸、酯的性质及应用,题目难度不大.

练习册系列答案
相关题目
5.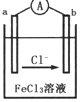 某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )
某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )
 某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )
某化学兴趣小组利用反应Zn+2FeC13═ZnCl2+2FeCl2,设计了如图所示的原电池装置,下列说法正确的是( )| A. | Zn为负极,发生还原反应 | |
| B. | b电极反应式为ZFe3++2e-═2Fe2+ | |
| C. | 电子流动方向是a电极→FeCl3溶液→b电极 | |
| D. | 电池的正极材料可以选用石墨、铂电极,也可以用铜电极 |
15.25℃时,下列溶液中的微粒浓度关系正确的是( )
| A. | pH=3的0.1mol•L-1的NaHC2O4溶液中:c(C2O42-)<c(H2C2O4) | |
| B. | 0.1mol•L-1的Na2S溶液中:2c(Na+)=c(S2-)+c(HS-)+c(H2S) | |
| C. | pH=4的CH3COOH溶液中:$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-10 | |
| D. | 等物质的量浓度、等体积的NaF溶液和HF溶液混合所得的稀溶液中:c(H+)+c(Na+)=c(F-)+c(OH-) |
12.下列化学方程式或离子方程式正确的是( )
| A. | Cu与S加热反应:Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | |
| B. | 向氯化氨的稀溶液中加入少量NaOH:NH${\;}_{4}^{+}$+OH=NH3↑+H2O | |
| C. | 向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ | |
| D. | SO2气体通入溴水中:SO2+Br2+2H2O=2Br-+SO${\;}_{4}^{2-}$+4H+ |
19. 如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )
 如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )| A. | X是负极,Y是正极 | B. | Cu电极逐渐溶解 | ||
| C. | CuSO4溶液的pH逐渐减小 | D. | CuSO4溶液的pH不变 |
9.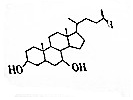 鹅去氧胆酸是目前世界上用量最大的治胆结石药物之一,其结构简式如图所示,下列关于鹅去氧胆酸的说法正确的是( )
鹅去氧胆酸是目前世界上用量最大的治胆结石药物之一,其结构简式如图所示,下列关于鹅去氧胆酸的说法正确的是( )
 鹅去氧胆酸是目前世界上用量最大的治胆结石药物之一,其结构简式如图所示,下列关于鹅去氧胆酸的说法正确的是( )
鹅去氧胆酸是目前世界上用量最大的治胆结石药物之一,其结构简式如图所示,下列关于鹅去氧胆酸的说法正确的是( )| A. | 分子中含有4个苯环 | |
| B. | 1mol鹅去氧胆酸和足量NaHCO3溶液反应产生3molCO2 | |
| C. | 不能使酸性KMnO4溶液褪色 | |
| D. | 能发生取代、氧化等反应 |
16.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 16gO2分子数为NA | |
| B. | 在常温常压下,22.4L氖气含有的原子数为NA | |
| C. | 1mol H2O在标准状况下所占有的体积约为22.4L | |
| D. | 1mol H2O2完全分解时,转移的电子总数为NA |
14.化学与社会、生活密切相关.下列说法正确的是( )
| A. | 稀豆浆、食盐水均可产生丁达尔效应 | |
| B. | 利用生物质能就是间接利用太阳能 | |
| C. | 钢铁在潮湿的空气中主要发生化学腐蚀 | |
| D. | 纯铝质轻,耐腐蚀性强,可直接用作航天材料 |
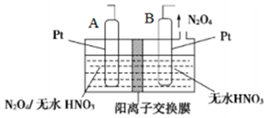 氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛.
氮的氧化物种类较多,有N2O、NO、N2O3、NO2、N2O4、N2O5等,他们应用广泛.