题目内容
在酸性溶液中能大量共存而且为无色透明的溶液是( )
| A、NH4+、Al3+、SO42-、NO3- |
| B、K+、Cu2+、Cl-、CO32- |
| C、K+、MnO4-、NH4+、NO3- |
| D、Na+、K+、HCO3-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:酸性溶液中存在大量氢离子,溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.NH4+、Al3+、SO42-、NO3-离子之间不满足离子反应发生条件;
B.铜离子为有色离子,铜离子与碳酸根离子反;
C.高锰酸根离子为有色离子,不满足溶液无色的要求;
D.碳酸氢根离子与氢离子反应生成二氧化碳气体和水.
A.NH4+、Al3+、SO42-、NO3-离子之间不满足离子反应发生条件;
B.铜离子为有色离子,铜离子与碳酸根离子反;
C.高锰酸根离子为有色离子,不满足溶液无色的要求;
D.碳酸氢根离子与氢离子反应生成二氧化碳气体和水.
解答:
解:A、NH4+、Al3+、SO42-、NO3-离子之间不反应,在溶液中能大量共存,故A正确;
B、Cu2+在水溶液显蓝色,Cu2+和CO32-反应生成沉淀,在溶液中不能大量共存,故B错误;
C、MnO4-在水溶液中显紫色,在溶液中不能共存,故C错误;
D、酸性溶液中H+和HCO3-反应生成水和二氧化碳,在溶液中不能共存,故D错误;
故选A.
B、Cu2+在水溶液显蓝色,Cu2+和CO32-反应生成沉淀,在溶液中不能大量共存,故B错误;
C、MnO4-在水溶液中显紫色,在溶液中不能共存,故C错误;
D、酸性溶液中H+和HCO3-反应生成水和二氧化碳,在溶液中不能共存,故D错误;
故选A.
点评:本题考查离子共存的判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O下列说法正确的( )
| ||
| A、H2C2O4在反应中被氧化 |
| B、KClO3在反应中得到电子 |
| C、CO2是还原产物 |
| D、4 molKClO3参加反应有8 mol电子转移 |
下列盐中,既不是碱式盐,也不是酸式盐的是( )
| A、NaHSO4 |
| B、Cu2(OH)2CO3 |
| C、NH4NO3 |
| D、Ca(H2PO4)2 |
A、B、C、D、E均含有同一种短周期元素,其中A是单质,B常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物.下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是:( )
| 物质 编号 | 物质转化关系 | A | D | E |
| ① | 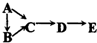 | Si | SiO2 | H2SiO3 |
| ② | N | NO2 | HNO3 | |
| ③ | S | SO2 | H2SO4 | |
| ④ | Na | Na2O2 | NaOH |
| A、①②③④ | B、②③ |
| C、①③④ | D、②④ |
氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性.下列叙述中不正确( )
| A、红热的铜丝在氯气中剧烈燃烧,生成棕黄色烟 |
| B、钠在氯气中燃烧,生成白色的烟 |
| C、纯净的氢气在氯气中安静的燃烧,在集气瓶口形成白色烟雾 |
| D、氯气能与水反应生成盐酸和次氯酸,次氯酸见光易分解 |
下列离子方程式正确的是( )
| A、铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO2-+H2↑ |
| B、铜跟稀硝酸反应:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
| C、硫酸铜溶液和氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ |
| D、实验室用大理石和稀盐酸制取CO2:2H++CO32-═CO2↑+H2O |