题目内容
(1)纯净物根据其组成和性质可进行如下分类:
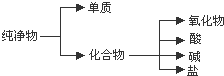
如图所示的分类方法属于 (填序号)
A.交叉分类法 B.树状分类法
(2)下列2组物质中均有一种物质的类别与其它2种不同
A.CaO、Na2O、SiO2 B.HClO、HCl、H2SO4
以上两组物质中,每组里与别的物质不同的物质依次是(填化学式) .
(3)写出下列反应的离子方程式:
①Cu(OH)2与盐酸反应
②MnO2+4HCl═MnCl2+Cl2↑+2H2O
(4)将下列离子方程式改写成化学方程式:
①CO32-+2H+═CO2↑+H2O
②Fe+Cu2+═Fe2++Cu .

如图所示的分类方法属于
A.交叉分类法 B.树状分类法
(2)下列2组物质中均有一种物质的类别与其它2种不同
A.CaO、Na2O、SiO2 B.HClO、HCl、H2SO4
以上两组物质中,每组里与别的物质不同的物质依次是(填化学式)
(3)写出下列反应的离子方程式:
①Cu(OH)2与盐酸反应
②MnO2+4HCl═MnCl2+Cl2↑+2H2O
(4)将下列离子方程式改写成化学方程式:
①CO32-+2H+═CO2↑+H2O
②Fe+Cu2+═Fe2++Cu
考点:离子方程式的书写,酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题,离子反应专题
分析:(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,之间为包含关系;
(2)A、根据氧化物的组成元素来判断物质的类别;
B、根据是否含氧酸可以分为含氧酸和无氧酸;
(3)①Cu(OH)2与盐酸反应生成氯化铜和水;
②根据离子方程拆分原则解答;
(4)①CO32-+2H+═CO2↑+H2O表示可溶性碳酸盐和强酸反应;
②Fe+Cu2+═Fe2++Cu表示铁与可溶性铜盐反应生成铜和二价铁离子.
(2)A、根据氧化物的组成元素来判断物质的类别;
B、根据是否含氧酸可以分为含氧酸和无氧酸;
(3)①Cu(OH)2与盐酸反应生成氯化铜和水;
②根据离子方程拆分原则解答;
(4)①CO32-+2H+═CO2↑+H2O表示可溶性碳酸盐和强酸反应;
②Fe+Cu2+═Fe2++Cu表示铁与可溶性铜盐反应生成铜和二价铁离子.
解答:
解:(1)树状分类法是一种很形象的分类法,按照层次,一层一层来分,就像一棵大树,图示方法就是树状图,故B选;
A.CaO、Na2O为金属氧化物,SiO2 为非金属氧化物,故选:SiO2;
B.H2SO4、HClO为含氧酸,HCl为无氧酸,故选HCl;
故答案为:SiO2、HCl;B;
(3)①Cu(OH)2与盐酸反应,离子方程式为:Cu2++2OH-═Cu(OH)2↓;
故答案为:Cu2++2OH-═Cu(OH)2↓;
②MnO2+4HCl═MnCl2+Cl2↑+2H2O,离子方程式为:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O;
故答案为:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O;
(4)①CO32-+2H+═CO2↑+H2O可以表示碳酸钠和盐酸反应,化学方程式为:Na2CO3+2HCl═CO2↑+H20+2NaCl,
故答案为:Na2CO3+2HCl═CO2↑+H20+2NaCl;
②Fe+Cu2+═Fe2++Cu可以表示铁与氯化铜反应,化学方程式为:Fe+CuCl2═FeCl2+Cu,
故答案为:Fe+CuCl2═FeCl2+Cu.
A.CaO、Na2O为金属氧化物,SiO2 为非金属氧化物,故选:SiO2;
B.H2SO4、HClO为含氧酸,HCl为无氧酸,故选HCl;
故答案为:SiO2、HCl;B;
(3)①Cu(OH)2与盐酸反应,离子方程式为:Cu2++2OH-═Cu(OH)2↓;
故答案为:Cu2++2OH-═Cu(OH)2↓;
②MnO2+4HCl═MnCl2+Cl2↑+2H2O,离子方程式为:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O;
故答案为:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O;
(4)①CO32-+2H+═CO2↑+H2O可以表示碳酸钠和盐酸反应,化学方程式为:Na2CO3+2HCl═CO2↑+H20+2NaCl,
故答案为:Na2CO3+2HCl═CO2↑+H20+2NaCl;
②Fe+Cu2+═Fe2++Cu可以表示铁与氯化铜反应,化学方程式为:Fe+CuCl2═FeCl2+Cu,
故答案为:Fe+CuCl2═FeCl2+Cu.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
下列各反应中,氧化反应与还原反应在同种元素中进行的是( )
| A、Cl2+2NaOH=NaCl+NaClO+H2O | ||||
B、2KClO3
| ||||
C、2KMnO4
| ||||
D、2H2O
|
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,5.6L氯气和16.8L氧气的混合气体中含有分子数为NA |
| B、标准状况下,22.4LH2O所含有原子数为3NA |
| C、NA个N2分子所占的体积与0.5 NA个H2分子所占的体积比一定是2:1 |
| D、1.8g的NH4+离子中含有的电子数1.1NA |
在酸性溶液中能大量共存而且为无色透明的溶液是( )
| A、NH4+、Al3+、SO42-、NO3- |
| B、K+、Cu2+、Cl-、CO32- |
| C、K+、MnO4-、NH4+、NO3- |
| D、Na+、K+、HCO3-、NO3- |
能正确表示下列反应的离子方程式为( )
| A、碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH-=CO32-+H2O |
| B、二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O |
| C、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
| D、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
若X、Y为同周期元素,且电负性X>Y,下列说法肯定错误的是( )
| A、X与Y形成化合物时,X显负价,Y显正价 |
| B、X的第一电离能大于Y |
| C、X的原子序数小于Y |
| D、气态氢化物的稳定性X强于Y |
下列各组离子在指定环境下能大量共存的是( )
| A、pH=1的溶液中:Na+、S2-、K+、MnO4- |
| B、pH=7的溶液中:Al3+、Cl-、SO42-、HCO3- |
| C、pH>7的溶液中:Na+、AlO2-、SO42-、K+ |
| D、pH=0的溶液中:Na+、K+、Fe2+、ClO- |