题目内容
下列反应中可用离子方程式H++OH-═H2O表示的是( )
| A、NH4Cl+NaOH═NaCl+NH3?H2O |
| B、Mg(OH)2+2HCl═MgCl2+2H2O |
| C、NaOH+NaHCO3═Na2CO3+H2O |
| D、NaOH+HNO3═NaNO3+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成的一水合氨属于弱电解质,离子方程式中保留分子式;
B.氢氧化镁为难溶物,在离子反应中保留化学式;
C.碳酸氢根为二元弱酸碳酸的酸根离子,在离子反应中不能拆分;
D.氢氧化钠和硝酸都为可溶性的强电解质,可拆写.
B.氢氧化镁为难溶物,在离子反应中保留化学式;
C.碳酸氢根为二元弱酸碳酸的酸根离子,在离子反应中不能拆分;
D.氢氧化钠和硝酸都为可溶性的强电解质,可拆写.
解答:
解:A.反应的离子方程式为:NH4++OH-═+NH3?H2O,不能够用离子方程式H++OH-=H2O表示,故A错误;
B.反应的离子方程式为:Mg(OH)2+2H+═Mg2++2H2O,不能够用离子方程式H++OH-=H2O表示,故B错误;
C.反应的离子方程式为:HCO3-+OH-═CO32-+H2O,不能够用离子方程式H++OH-=H2O表示,故C错误;
D.反应生成硝酸钠和水,可用H++OH-=H2O表示,故D正确;
故选D.
B.反应的离子方程式为:Mg(OH)2+2H+═Mg2++2H2O,不能够用离子方程式H++OH-=H2O表示,故B错误;
C.反应的离子方程式为:HCO3-+OH-═CO32-+H2O,不能够用离子方程式H++OH-=H2O表示,故C错误;
D.反应生成硝酸钠和水,可用H++OH-=H2O表示,故D正确;
故选D.
点评:本题考查了离子方程的书写,侧重考查了反应的实质应用,氢离子和氢氧根离子反应的离子方程式是溶液能全部电离出氢离子和全部电离出氢氧根离子的物质间的反应.要求学生掌握离子方程式的书写方法,该题有助于培养学生分析问题、解决问题的能力,题目难度中等.

练习册系列答案
相关题目
如图所示, 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
为电镀槽.接通电路(未闭合K)后发现 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
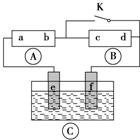
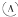 为直流电源,
为直流电源,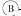 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路(未闭合K)后发现
为电镀槽.接通电路(未闭合K)后发现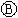 上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( )
上的c点显红色.为实现铁上镀铜,使c、d两点短路.下列叙述不正确的是( ) 
| A、b为直流电源的负极 |
| B、f极为阴极,发生还原反应 |
| C、e极材料为铁片,f极材料的铜片 |
| D、可选用CuSO4溶液或CuCl2溶液作电镀液 |
下列离子方程式不正确的是( )
| A、向氢氧化钾溶液中滴加少量氯化铝溶液 Al3++4OH-=AlO2-+2H2O |
| B、在亚硫酸中加入过量的次氯酸钠溶液 H2SO3+3ClO-=Cl-+2HClO+SO42- |
| C、在稀HNO3溶液加入FeS固体 FeS+2H+=Fe2++H2S↑ |
| D、在过氧化钠中加入稀硫酸 2Na2O2+4H+=4Na++2H2O+O2↑ |
 某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.甲同学认为两者反应只生成CuCO3一种沉淀;乙同学认为这两者相互促进水解,只生成Cu(OH)2一种沉淀;丙同学认为生成CuCO3和Cu(OH)2两种沉淀.(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.甲同学认为两者反应只生成CuCO3一种沉淀;乙同学认为这两者相互促进水解,只生成Cu(OH)2一种沉淀;丙同学认为生成CuCO3和Cu(OH)2两种沉淀.(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)