题目内容
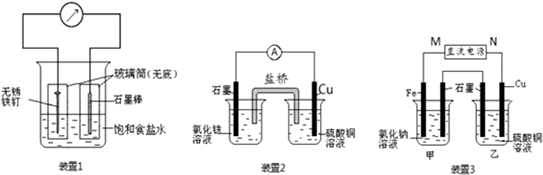
15.下列装置属于工作中的电解池(其中C表示石墨)的是( )| A. |  | B. |  | C. |  | D. |  |
分析 属于电解池,应外加电源,题中属于工作中的电解池,应形成闭合回路,且电极发生反应,以此解答该题.
解答 解:A.乙醇不导电,不能形成电解池,故A错误;
B.没有外加电源,不是电解池,故B错误;
C.外加电源,为电解池,形成闭合回路,可发生电极反应,故C正确;
D.电路没有闭合,电解池不能正常工作,故D错误.
故选C.
点评 本题考查电解原理,为高频考点,侧重于学生的分析能力的考查,注意把握电解池的组成以及工作原理,难度不大.

练习册系列答案
 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
5.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有7个电子,Y原子最外层电子数是最内层电子数的一半,Z最高正价是最低负价绝对值的3倍.下列叙述正确的是( )
| A. | Y的离子半径比X的离子半径大 | |
| B. | 化合物Y2Z中既有离子键、又有共价键 | |
| C. | Y、W最高价氧化物对应水化物的溶液均能溶解氧化铝 | |
| D. | 简单气态氢化物的稳定性由强到弱的顺序:Z、W、X |
3.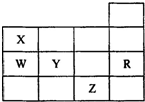 表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是( )
表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是( )
 表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是( )
表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是( )| A. | 常温常压下,五种元素的单质中有两种是气态 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | W的氢化物比X的氢化物沸点高 | |
| D. | Y与W元素的最高价氧化物对应的水化物的酸性比较,前者弱于后者 |
10.在一定温度下,下列叙述不是可逆反应A(g)+3B(g)?2C(g)达到平衡的标志的是( )
| A. | C的生成速率与C的分解速率相等 | |
| B. | 单位时间内生成a mol A,同时生成3a mol B | |
| C. | A、B、C的浓度不再变化 | |
| D. | 混合气体的总压强不再变化 |
7.在PH=13的溶液中,下列各离子组可以大量共存的是( )
| A. | Na+、NO3-、H+、Ag+ | B. | K+、Fe3+、Cl-、SO42- | ||
| C. | K+、Ba2+、Cl-、CO32- | D. | Na+、AlO2-、K+、Cl- |
4.化学与人类生活密切相关,下列说法不正确的是( )
| A. | 大量燃烧化石燃料及汽车尾气是造成雾霾天气的重要因素 | |
| B. | 冬天严禁在窗门紧闭的室内用煤饼炉取暖,因为生成的CO、SO2等容易引起中毒 | |
| C. | 为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰 | |
| D. | 氯气泄露时,应用蘸有肥皂水的湿毛巾捂住口鼻疏散到安全地带 |
5.下列反应属于氧化还原反应的是( )
| A. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | B. | Na2O+H2O═2NaOH | ||
| C. | 4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O | D. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |