题目内容
对于在密闭容器中进行的反应:N2+O2?2ΝΟ,下列不能加快该反应的反应速率的条件是( )
| A、缩小体积 |
| B、充入更多的NO |
| C、体积增大到原来的2倍 |
| D、升高温度 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:影响化学反应速率快慢的因素有内因和外因,反应物本身的性质(内因),温度、浓度、压强、催化剂等为影响化学反应速率的外界因素,对于反应N2+O2?2NO是一个反应前后体积不变的反应,据此结合选项的内容解答.
解答:
解:A.缩小体积,反应物的浓度增大,活化分子的数目增多,能使反应速率增大,故A错误;
B.体积不变充入NO,对于反应N2+O2?2NO,生成物的浓度增大,活化分子的数目增多,能使反应速率增大,故B错误;
C.体体积增大到原来的2倍各组分浓度减小,会使反应速率减慢,故C正确;
D.温度升高,反应物获得能量,增大活化分子数,反应速率加快,故D错误;
故选C.
B.体积不变充入NO,对于反应N2+O2?2NO,生成物的浓度增大,活化分子的数目增多,能使反应速率增大,故B错误;
C.体体积增大到原来的2倍各组分浓度减小,会使反应速率减慢,故C正确;
D.温度升高,反应物获得能量,增大活化分子数,反应速率加快,故D错误;
故选C.
点评:本题考查影响化学反应速率的外界因素的适用范围,明确温度、压强、浓度、催化剂等常见的对反应的影响因素是解答的关键,题目较简单.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
一学生用如图装置研究原电池原理,下列说法错误的是( )

| A、(3)图中Zn片增重质量与Cu棒减轻质量的比值为65:64 |
| B、(2)图中如果两极上都有气体产生,则说明Zn片不纯 |
| C、(1)图中铜棒上没有气体产生 |
| D、(2)图与(3)图中正极生成物质质量比为1:32时,Zn棒减轻的质量相等 |
合成聚氯乙烯,下列的说法正确的是( )
| A、用食盐、水和乙烯为原料可以合成聚氯乙烯 |
| B、用氯气和乙炔为原料可以直接合成聚氯乙烯 |
| C、合成聚氯乙烯一定涉及氧化还原反应 |
| D、合成聚氯乙烯一定涉及加成聚合反应 |
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池.若a、b相连时,a为负极;c、d相连时,电流流向为d→导线→c;a、c相连时,c极上产生大量气泡;b、d相连时,b极上发生还原反应.则四种金属的活动性顺序由强到弱的顺序为( )
| A、a>c>d>b |
| B、c>a>b.>d |
| C、a>b>c>d |
| D、b>d>c>a |
已知断裂1mol H2和1mol Cl2中的化学键吸收的能量分别为436kJ、243kJ,而由H原子和Cl原子形成1mol HCl时释放的能量为431kJ.则下列热化学方程式中正确的是( )
A、
| ||||
| B、H2(g)+Cl2(g)═2HCl(g);△H=-183 kJ?mol-1 | ||||
C、HCl(g)═
| ||||
| D、H2(g)+Cl2(g)═2HCl(g);△H=+248 kJ?mol-1 |

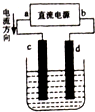 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.