题目内容
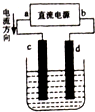 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.(1)正极为
(2)阳极电极反应式为
(3)电解一段时间后发现阴极增重6.4g,则外电路中通过的电子的物质的量是
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)电解CuCl2溶液的装置,其中c、d为石墨电极,依据电流流向可知,电源电极a为正极,与a连接的电极c为电解池的阳极;b为负极,与b电极相连的电极d为电解池的阴极;
(2)阳极是c电极,溶液中氯离子失电子生成氯气,依据氯气使湿润的淀粉碘化钾试纸放在c电极附近,若试纸变蓝,则证明产生的气体为氯气;
(3)依据电极反应计算反应过程中的电子转移数.
(2)阳极是c电极,溶液中氯离子失电子生成氯气,依据氯气使湿润的淀粉碘化钾试纸放在c电极附近,若试纸变蓝,则证明产生的气体为氯气;
(3)依据电极反应计算反应过程中的电子转移数.
解答:
解:(1)电解CuCl2溶液的装置,其中c、d为石墨电极,依据电流流向可知,电源电极a为正极,与a连接的电极c为电解池的阳极;b为负极,与b电极相连的电极d为电解池的阴极,
故答案为:a;c;
(2)阳极是c电极,溶液中氯离子在阳极失电子发生氧化反应,电极反应为:2Cl-一2e一=C12↑;生成的氯气用湿润的淀粉碘化钾试纸放在c电极附近,若试纸变蓝,则证明产生的气体为氯气;
故答案为:2Cl-一2e一=C12↑;用湿润的淀粉碘化钾试纸放在c电极附近,若试纸变蓝,则证明产生的气体为氯气;
(3)电解一段时间后发现阴极增重6.4g,依据离子放电顺序溶液中铜离子得到电子生成铜,物质的量=
=0.1mol,电极反应为:Cu2++2e-=Cu,电子转移0.2mol,外电路中通过的电子的物质的量是0.2mol,
故答案为:0.2mol.
故答案为:a;c;
(2)阳极是c电极,溶液中氯离子在阳极失电子发生氧化反应,电极反应为:2Cl-一2e一=C12↑;生成的氯气用湿润的淀粉碘化钾试纸放在c电极附近,若试纸变蓝,则证明产生的气体为氯气;
故答案为:2Cl-一2e一=C12↑;用湿润的淀粉碘化钾试纸放在c电极附近,若试纸变蓝,则证明产生的气体为氯气;
(3)电解一段时间后发现阴极增重6.4g,依据离子放电顺序溶液中铜离子得到电子生成铜,物质的量=
| 6.4g |
| 64g/mol |
故答案为:0.2mol.
点评:本题考查了电解池原理的分析判断,依据电流流向分析判断电极名称,书写电极反应是关键,题目难度中等.

练习册系列答案
相关题目
 化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示.下列说法不正确的是( )
化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示.下列说法不正确的是( )| A、A为电源正极 |
| B、阳极反应式为:2H2O-4e-═4H++O2↑ |
| C、若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为10.4克 |
| D、阴极反应式为:2NO3-+6H2O+10e-=N2↑+12OH- |
下列离子在溶液中能大量共存的是( )
| A、CO32-、Na+、SO42-、H+ |
| B、Cu2+、SO42-、H+、Cl- |
| C、K+、OH-、NO3-、HCO3- |
| D、Al3+、NO3-、SO42-、OH- |
对于在密闭容器中进行的反应:N2+O2?2ΝΟ,下列不能加快该反应的反应速率的条件是( )
| A、缩小体积 |
| B、充入更多的NO |
| C、体积增大到原来的2倍 |
| D、升高温度 |
下列有关同分异构体数目的叙述中,不正确的是( )
| A、甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| B、分子式符合C5H11Cl的化合物有6种 |
| C、已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种 |
D、菲的结构简式为 ,它与硝酸反应,可生成5种一硝基取代物 ,它与硝酸反应,可生成5种一硝基取代物 |
下列说法中正确的是( )
| A、500mL 1mol?L-1 MgCl2溶液中含有Cl-数目为0.5NA |
| B、标准状况下,1mol H2O与1mol O2所占的体积相等 |
| C、1mol S与足量Cu反应生成Cu2S,转移的电子数为NA |
| D、常温常压下,1mol氦气所含的原子数为NA |