题目内容
16.将SO2气体通入下列溶液中,观察不到明显现象的是( )| A. | BaCl2 | B. | 石蕊溶液 | C. | 酸性KMnO4溶液 | D. | 氢硫酸 |
分析 依据二氧化硫具有强的还原性,弱的氧化性,为酸性氧化物,具有酸性氧化物的通性的性质解答.
解答 解:A.盐酸的反应大于亚硫酸,则二者不反应,无明显现象,故A选;
B.二氧化硫为酸性氧化物,能与水反应生成亚硫酸,亚硫酸电离产生氢离子,能够使石蕊变红色,故B不选;
C.二氧化硫具有强的还原剂性,能够还原高锰酸钾,使其褪色,故C不选;
D.二氧化硫具有弱的氧化性,能够氧化硫化氢,生成单质硫,产生沉淀,故D不选;
故选:A.
点评 本题考查二氧化硫的化学性质,为高频考点,明确二氧化硫酸性氧化物、强的还原性、弱的氧化性的性质是解题关键,题目难度不大.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
3.下列离子检验的步骤、现象和结论都正确的是( )
| A. | 向试液中滴加氯化钡溶液,产生白色沉淀,则溶液中一定含有CO32- | |
| B. | 向试液中滴加浓氢氧化钠溶液,加热产生刺激性气味的气体,则溶液中一定含有NH4+ | |
| C. | 向试液中滴加硝酸银溶液,产生白色沉淀,则溶液中一定含有Cl- | |
| D. | 向试液中滴加盐酸,产生的气体能使品红溶液褪色,则溶液中一定含有SO32- |
7.等物质的量的钠、铁、铝分别与足量的盐酸充分反应,在相同的条件下,产生氢气的体积比是( )
| A. | 1:1:1 | B. | 1:3:3 | C. | 1:2:3 | D. | 2:3:3 |
4.下列对同系物归纳错误的是( )
| A. | 同系物都符合同一通式 | |
| B. | 同系物彼此在组成上相差一个或若干个某种原子团 | |
| C. | 同系物具有相同的最简式 | |
| D. | 同系物的结构相似 |
11.对于反应:KClO3+6HCl→KCl+3Cl2↑+3H2O,若有0.1molKClO3参加反应,下列说法正确的是( )
| A. | 被氧化的 HCl为0.6mol | B. | 转移电子1.806×1023个 | ||
| C. | 产生气体为6.72L | D. | 还原剂占参加反应HCl的$\frac{5}{6}$ |
1.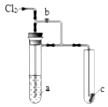 将氯气通入如图装置.若打开活塞,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,c很快褪色.则a溶液可能是( )
将氯气通入如图装置.若打开活塞,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,c很快褪色.则a溶液可能是( )
 将氯气通入如图装置.若打开活塞,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,c很快褪色.则a溶液可能是( )
将氯气通入如图装置.若打开活塞,则小试管里的干燥品红试纸c不褪色;若关闭活塞b,c很快褪色.则a溶液可能是( )| A. | 浓FeCl2溶液 | B. | 饱和KI溶液 | C. | 饱和食盐水 | D. | 浓NaOH溶液 |
8.25℃时,将两种不同浓度的某一元酸HA分别与NaOH溶液等体积混合(混合后溶液体积等于混合前两溶液体积之和),测得反应后溶液的pH如表所示.下列判断错误的是( )
| 实验编号 | 起始浓度 (mol/L) | 反应后溶液的pH | |
| C(HA) | C(NaOH) | ||
| ① | 0.10 | 0.10 | 9 |
| ② | x | 0.05 | 7 |
| A. | HA是弱酸 | |
| B. | x>0.05 | |
| C. | 实验①所得溶液中:c(A-)+c(HA)=0.10mol/L | |
| D. | 实验②所得溶液中:c(Na+)=c(A-) |
5.工业上生产乙烯、丙烯的主要方法是( )
| A. | 裂化 | B. | 干馏 | C. | 分馏 | D. | 裂解 |
6.以下离子中,半径最大的是( )
| A. | Na+ | B. | K+ | C. | S2- | D. | Cl- |