题目内容
12.下列关于苯的性质的叙述中,不正确的是( )| A. | 苯是无色且带有特殊气味的液体 | |
| B. | 常温下苯是一种不溶于水且密度小于水的液体 | |
| C. | 苯在一定条件下能与溴发生取代反应 | |
| D. | 苯分子中不含碳碳双键,不可能发生加成反应 |
分析 苯是无色有特殊气味的气体,密度比水小,难溶于水,苯中碳碳键是介于单键和双键之间的独特的键,故苯能发生取代反应和加成反应,如苯的溴代,苯与氢气的加成,
解答 解:A.苯是无色有特殊气味,故A正确;
B.苯的密度比水小,是难溶于水的液体,故B正确;
C.苯在铁作催化剂的条件下苯中氢原子被溴原子取代生成溴苯与溴化氢,发生取代反应,故C正确;
D.苯中的化学键是一个大π键,能发生取代反应和加成反应,如苯的溴代,苯与氢气的加成,故D错误.
故选D.
点评 本题主要考查了苯的结构与性质,题目难度不大,注意苯中的化学键是既不同于碳碳单键也不同于碳碳双键的大π键.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
2.反应mA(g)+nB(g)?pC(g)+qD(g)经10min后达到平衡,测得此时A的浓度减少了n mol•L-1,C的浓度增加了$\frac{2}{3}$ n mol•L-1,又知,平均反应速率vc=2vB.达到平衡后,若保持温度不变,缩小容器体积,A的转化率不变,那么该反应的化学方程式应为( )
| A. | 2A(g)+6B(g)?3C(g)+5D(g) | B. | 3A(g)+B(g)?2C(g)+2D(g) | C. | 3A(g)+B(g)?C(g)+D(g) | D. | A(g)+3B(g)?3C(g)+3D(g) |
3.下列操作中,能使电离平衡H2O?H++OH-,向右移动且溶液呈酸性的是( )
| A. | 向水中加入KHSO4溶液 | B. | 将水加热到100℃,使pH=6 | ||
| C. | 向水中加入Na3PO4溶液 | D. | 向水中加入ZnSO4固体 |
20.设NA为阿伏伽德罗常数,下列说法中正确的是( )
| A. | 1molNa2O2固体中含阴离子个数为2NA | |
| B. | 1molSiO2中含Si-O的数目为2NA | |
| C. | 标准状况下,22.4L乙炔中含π键数为2NA | |
| D. | 1molNaHCO3晶体中阳离子数为2NA |
7.下列事实及解释的化学(或离子)方程式均正确的是( )
| A. | MnCl2溶液中常含有Cu2+,可添加难溶电解质MnS除去:Cu2++S2-=CuS↓ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞是因为:SiO2+2OH-=SiO32-+H2O | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 向氨水中滴入少量饱和氯化铁溶液制各Fe(OH)3胶体:Fe3++3NH3•H2O?Fe(OH)3(胶体)+3NH4+ |
17.同温同压下,等质量的SO2和CO2,正确的叙述是( )
| A. | 分子数之比1:1 | B. | 密度之比4:11 | C. | 密度之比11:16 | D. | 体积之比11:16 |
4.下列实验操作合理的是( )
| A. |  用标准液滴定待测液 | B. |  检查装置气密性 | ||
| C. | 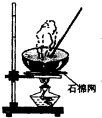 蒸发 | D. |  读取气体体积 |
1.有A、B、C、D四种金属,将A、B用导线连接后浸在稀硫酸中,A上放出氢气,B逐渐溶解生成B2+;在含 A2+和C2+的混合溶液中加入铁,铁棒先析出C;将D放入B2+的硝酸盐溶液中,D表面有B析出.这四种金属阳离子的氧化性由强到弱的顺序是( )
| A. | D2+>B2+>A2+>C2+ | B. | A2+>B2+>C2+>D2+ | C. | C2+>A2+>B2+>D2+ | D. | A2+>C2+>D2+>B2+ |