题目内容
8.G是某抗炎症药物的中间体,其合成路线如下: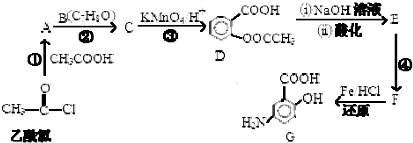
已知:
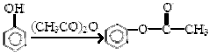 ,
, (具有还原性,极易被氧化)
(具有还原性,极易被氧化)(1)B的结构简式为
 .
.(2)反应④的条件为浓硫酸、浓硝酸、加热;①的反应类型为取代反应;反应②的作用是保护酚羟基,以防被氧化.
(3)下列对有机物G的性质推测正确的是AC(填选项字母).
A.具有两性,既能与酸反应也能和碱反应
B.能发生消去反应、取代反应和氧化反应
C.能聚合成高分子化合物
D.1molG与足量NaHCO3溶液反应放出2molCO2
(4)D与足量的NaOH反应的化学方程式为
 .
.(5)符合下列条件的C的同分异构体有16种
a.属于芳香族化合物,且含有两个甲基
b.能发生银镜反应
c.与FeCl3溶液发生显色反应
其中核磁共振氢谱有4组峰,且峰面积之比为6:2:1:1的是
 (写出其中一种结构简式)
(写出其中一种结构简式)(6)已知:苯环上有烷烃基时,新引入的取代基连在苯环的邻对位;苯环上有羧基时,新引入的取代基连在苯环的间位.根据题中的信息,写出以甲苯为原料合成有机物
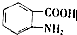 的流程图(无机试剂任选).合成路线流程图如下:X$→_{反应条件}^{反应物}$Y$→_{反应条件}^{反应物}$Z…目标产物.
的流程图(无机试剂任选).合成路线流程图如下:X$→_{反应条件}^{反应物}$Y$→_{反应条件}^{反应物}$Z…目标产物.
分析 乙酰氯和乙酸反应生成A,A和B反应生成C,C被酸性高锰酸钾溶液氧化生成D,根据D结构简式知,B为 ,C为
,C为 ,A为CH3COOH,D发生水解反应然后酸化得到E,E为
,A为CH3COOH,D发生水解反应然后酸化得到E,E为 ,E反应生成F,F发生还原反应生成G,根据G结构简式结合题给信息知,F为
,E反应生成F,F发生还原反应生成G,根据G结构简式结合题给信息知,F为 ,
,
(6)甲苯和浓硝酸发生取代反应生成邻硝基甲苯,邻硝基甲苯被酸性高锰酸钾溶液氧化生成邻硝基苯甲酸,邻硝基苯甲酸被还原生成邻氨基苯甲酸,据此分析解答.
解答 解:乙酰氯和乙酸反应生成A,A和B反应生成C,C被酸性高锰酸钾溶液氧化生成D,根据D结构简式知,B为 ,C为
,C为 ,A为CH3COOH,D发生水解反应然后酸化得到E,E为
,A为CH3COOH,D发生水解反应然后酸化得到E,E为 ,E反应生成F,F发生还原反应生成G,根据G结构简式结合题给信息知,F为
,E反应生成F,F发生还原反应生成G,根据G结构简式结合题给信息知,F为 ,
,
(1)B的结构简式为 ,故答案为:
,故答案为: ;
;
(2)反应④的条件为浓硫酸、浓硝酸和加热;①的反应类型为取代反应;反应②的作用是保护酚羟基,防止被氧化,故答案为:浓硫酸、浓硝酸和加热;取代反应;保护酚羟基,防止被氧化;
(3)A.G中含有羧基和氨基,所以具有酸性和碱性,则具有两性,既能与酸反应也能和碱反应,故正确;
B.含有酚羟基,能发生氧化反应,不能发生消去反应,羧基能发生取代反应,故错误;
C.含有羧基和酚羟基,所以能发生缩聚反应生成高分子化合物,故正确;
D.只有羧基能和碳酸氢钠反应生成二氧化碳,所以1molG与足量NaHCO3溶液反应放出1molCO2,故错误;
故选AC;
(4)D与足量的NaOH反应的化学方程式为 ,故答案为:
,故答案为: ;
;
(5)C为 ,C的同分异构体符合下列条件:
,C的同分异构体符合下列条件:
a.属于芳香族化合物,说明含有苯环,且含有两个甲基;
b.能发生银镜反应,说明含有醛基;
c.与FeCl3溶液发生显色反应,说明含有酚羟基;
如果两个-CH3位于邻位、-OH位于-CH3邻位,有3种;
如果两个-CH3位于邻位、-OH与一个-CH3间位,有3种;
如果两个-CH3位于间位,-OH位于两个-CH3中间,有2种;
如果两个-CH3位于间位,-OH与其中一个-CH3邻位,有3种;
如果两个-CH3位于间位,-OH与其中两个-CH3间位,有3种;
如果两个-CH3位于对位,-OH与其中一个-CH3邻位,有2种;
所以符合条件的同分异构体有16种;
其中核磁共振氢谱有4组峰,且峰面积之比为6:2:1:1的是 ,
,
故答案为:16; ;
;
(6)甲苯和浓硝酸发生取代反应生成邻硝基甲苯,邻硝基甲苯被酸性高锰酸钾溶液氧化生成邻硝基苯甲酸,邻硝基苯甲酸被还原生成邻氨基苯甲酸,其合成流程图为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断和合成,为高频考点,侧重考查学生分析判断、知识迁移及知识综合应用能力,明确物质结构和性质、有机反应类型及反应条件是解本题关键,难点是同分异构体种类判断,题目难度中等.

 心算口算巧算一课一练系列答案
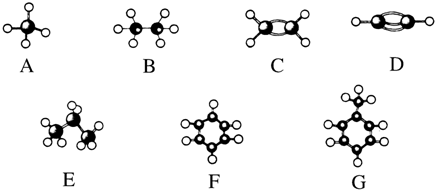
心算口算巧算一课一练系列答案| A. | 比丁烷更易液化 | B. | 是石油分馏的一种产品 | ||
| C. | 光照下能够发生取代反应 | D. | 分子中碳原子一定在同一平面上 |
| A. | 1mol•L-1 的AlCl3溶液中,含Al3+数小于NA | |
| B. | 标准状况下,将2.24L 氯化氢溶于足量水中,溶液中含有的HCl分子数为NA | |
| C. | 1mol NaBH4中含的离子的数目为6NA | |
| D. | 30g甲醛(HCHO)和醋酸的混合物中含碳原子数目为NA |
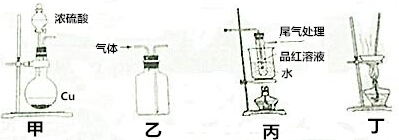
| A. | 用装置甲制取SO2 | |
| B. | 用装置乙制取SO2 | |
| C. | 用装置丙探究SO2与品红作用的可逆性 | |
| D. | 用装置丁蒸干硫酸铜溶液制得CuSO4•5H2O |
| 选项 | A | B | C | D |
| 实验装置图 |  | 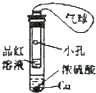 |  | 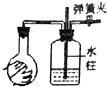 |
| 实验现象 | U形管右侧液面下降 | 小试管中品红溶液褪色 | 加入少量酚酞,溶液变浅红色 | 关闭弹簧夹,双手捂住圆底烧瓶,导管中水柱上升后静止不动 |
| 实验结论 | 该条件下铁钉发生吸氧腐蚀 | 证明二氧化硫具有还原性 | 证明Na2CO3能够发生水解 | 该装置气密性良好 |
| A. | A | B. | B | C. | C | D. | D |