题目内容
7.下列实验的有关叙述错误的是( )| 选项 | A | B | C | D |
| 实验装置图 |  | 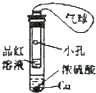 |  | 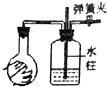 |
| 实验现象 | U形管右侧液面下降 | 小试管中品红溶液褪色 | 加入少量酚酞,溶液变浅红色 | 关闭弹簧夹,双手捂住圆底烧瓶,导管中水柱上升后静止不动 |
| 实验结论 | 该条件下铁钉发生吸氧腐蚀 | 证明二氧化硫具有还原性 | 证明Na2CO3能够发生水解 | 该装置气密性良好 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.U形管右侧液面下降,可知试管中气体减少;
B.Cu与浓硫酸反应需要加热;
C.碳酸钠溶液水解显碱性;
D.关闭弹簧夹,双手捂住圆底烧瓶,导管中水柱上升后静止不动,说明装置不漏气.
解答 解:A.U形管右侧液面下降,可知试管中气体减少,即氧气得到电子生成氢氧根离子,则该条件下铁钉发生吸氧腐蚀,故A正确;
B.Cu与浓硫酸反应需要加热,图中不能生成二氧化硫,且不能验证二氧化硫的漂白性、还原性,故B错误;
C.碳酸钠溶液水解显碱性,由现象加入少量酚酞,溶液变浅红色可知,发生了水解反应,故C正确;
D.关闭弹簧夹,双手捂住圆底烧瓶,导管中水柱上升后静止不动,说明装置不漏气,则该装置气密性良好,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高考常见题型,侧重于学生的分析能力、实验能力的考查,把握反应原理、实验装置的作用、实验基本操作和基本技能为解答该类题目的关键,注意实验现象与结论的关系,题目难度不大.

练习册系列答案
相关题目
18.在2L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(选填“吸热”、“放热”).反应达平衡后,若再通入一定量CO2,则平衡常数K将不变,CO2的转化率减小.(填“增大”、“减小”或“不变”)
(3)能判断该反应是否达到化学平衡状态的依据是bc(多选扣分).
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)若 600℃时,向容器中充入1mol CO、1mol H2O,反应达到平衡后,CO的转化率是$\frac{2}{3}$.
CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 600 | 800 | 830 | 1000 | 1200 |
| K | 0.25 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(选填“吸热”、“放热”).反应达平衡后,若再通入一定量CO2,则平衡常数K将不变,CO2的转化率减小.(填“增大”、“减小”或“不变”)
(3)能判断该反应是否达到化学平衡状态的依据是bc(多选扣分).
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)若 600℃时,向容器中充入1mol CO、1mol H2O,反应达到平衡后,CO的转化率是$\frac{2}{3}$.
19.下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4后,在试管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有砖红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体一定是乙烯 |
| D | 向水玻璃溶液中通入足量CO2 后,产生白色浑浊 | 生成了硅酸沉淀 |
| A. | A | B. | B | C. | C | D. | D |
17.青蒿素结构式如图所示.下列有关青蒿素的说法错误的是( )
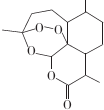

| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素分子结构稳定,受热不易分解 | |
| C. | 青蒿素可溶于NaOH溶液,可发生取代反应 | |
| D. | 青蒿素难溶于水,提取的方法是用有机溶剂萃取后蒸馏 |
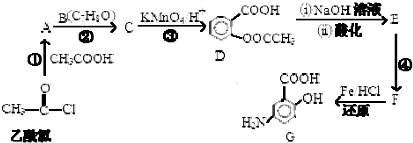
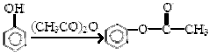 ,
, (具有还原性,极易被氧化)
(具有还原性,极易被氧化) .
. .
. (写出其中一种结构简式)
(写出其中一种结构简式)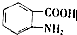 的流程图(无机试剂任选).合成路线流程图如下:X$→_{反应条件}^{反应物}$Y$→_{反应条件}^{反应物}$Z…目标产物.
的流程图(无机试剂任选).合成路线流程图如下:X$→_{反应条件}^{反应物}$Y$→_{反应条件}^{反应物}$Z…目标产物.