题目内容
(1)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活.
居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是 .
(2)氟氯代烷是一种能破坏臭氧层的物质.在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2 ②O3→O+O2 ③ClO+O→Cl+O2
上列的反应的总反应式是 ,(2分)少量氟氯代烷能破坏大量臭氧的原因是 .
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处.
①pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量,反应方程式为 .
②对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为 .
居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是
(2)氟氯代烷是一种能破坏臭氧层的物质.在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2 ②O3→O+O2 ③ClO+O→Cl+O2
上列的反应的总反应式是
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处.
①pH<
②对汽车加装尾气催化净化装置,可以使其中的NO、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为
考点:常见的生活环境的污染及治理
专题:元素及其化合物,化学应用
分析:(1)甲醛是来自人造地板、家具以及装修粘合剂,长期接触会引起过敏性皮炎,免疫功能异常;
(2)将方程式①②③相加得出氧气和臭氧的关系式;根据Cl+O3→ClO+O2 判断氟氯代烷能破坏大量臭氧的原因;
(3)①正常雨水中溶解二氧化碳,其pH=5.6,故pH值小于5.6的雨水为酸雨;酸雨主要是由化石燃料燃烧产生的二氧化硫、二氧化氮等酸性气体,经过复杂的大气化学反应形成;向煤中加入适量的CaCO3,可以大大减少燃物产物中SO2的量;
②根据质量守恒可知NO、CO相互反应转化成无毒的气体,生成氮气和二氧化碳,根据反应物与生成物来书写化学方程式.
(2)将方程式①②③相加得出氧气和臭氧的关系式;根据Cl+O3→ClO+O2 判断氟氯代烷能破坏大量臭氧的原因;
(3)①正常雨水中溶解二氧化碳,其pH=5.6,故pH值小于5.6的雨水为酸雨;酸雨主要是由化石燃料燃烧产生的二氧化硫、二氧化氮等酸性气体,经过复杂的大气化学反应形成;向煤中加入适量的CaCO3,可以大大减少燃物产物中SO2的量;
②根据质量守恒可知NO、CO相互反应转化成无毒的气体,生成氮气和二氧化碳,根据反应物与生成物来书写化学方程式.
解答:
解:(1)居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该物质是甲醛,
故答案为:甲醛;
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2;
氟氯代烷受紫外线的照射分解出氯原子,Cl+O3→ClO+O2,Cl对O3的分解有促进作用,所以能破坏臭氧层,
故答案为:2O3
3O2;氟氯代烷分解产生的Cl对O3的分解有促进作用;
(3)①空气中含有二氧化碳,二氧化碳能和雨水反应生成碳酸,正常雨水中溶解二氧化碳,饱和时其pH=5.6,故pH值小于5.6的雨水为酸雨,而二氧化硫、氮氧化物是形成酸雨的重要物质,其溶液的pH<5.6,向煤中加入适量的CaCO3,高温下石灰石分解生成CaO,可与SO2以及氧气反应生成硫酸钙,发生的反应为:2CaCO3+2SO2+O2
2CO2+2CaSO4,可以大大减少燃物产物中SO2的量,
故答案为:5.6;CaCO3;2CaCO3+2SO2+O2
2CO2+2CaSO4;
②由NO、CO相互反应转换成无毒的气体,即生成氮气和二氧化碳,该反应的化学反应方程式为2NO+2CO
N2+2CO2,故答案为:2NO+2CO
N2+2CO2.
故答案为:甲醛;
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2;
氟氯代烷受紫外线的照射分解出氯原子,Cl+O3→ClO+O2,Cl对O3的分解有促进作用,所以能破坏臭氧层,
故答案为:2O3
| ||
(3)①空气中含有二氧化碳,二氧化碳能和雨水反应生成碳酸,正常雨水中溶解二氧化碳,饱和时其pH=5.6,故pH值小于5.6的雨水为酸雨,而二氧化硫、氮氧化物是形成酸雨的重要物质,其溶液的pH<5.6,向煤中加入适量的CaCO3,高温下石灰石分解生成CaO,可与SO2以及氧气反应生成硫酸钙,发生的反应为:2CaCO3+2SO2+O2
| ||
故答案为:5.6;CaCO3;2CaCO3+2SO2+O2
| ||
②由NO、CO相互反应转换成无毒的气体,即生成氮气和二氧化碳,该反应的化学反应方程式为2NO+2CO
| ||
| ||
点评:本题考查较为综合,涉及粘合剂、氟氯代烷的催化以及环境保护等知识,为高频考点,侧重于化学与生活、环境的考查,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑ |
| B、用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-=Fe(SCN)3↓ |
| C、1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:2AlO2-+5 H+═Al(OH)3↓+Al3++H2O |
| D、碳酸氢钠溶液与少量氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
有CO2和NO的混和气体a mL,通过足量的Na2O2后,用排水法收集气体,结果没有收集到气体,则原混和气体中的CO2和NO的体积比为( )
| A、1:1 | B、1:2 |
| C、2:3 | D、3:2 |

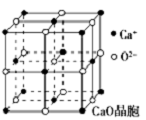 可以由下列反应合成三聚氰胺:CaO+3C
可以由下列反应合成三聚氰胺:CaO+3C )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸 (
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸 (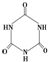 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过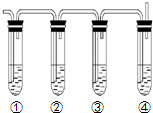 实验室制取乙烯的反应原理为:CH3CH2OH
实验室制取乙烯的反应原理为:CH3CH2OH