题目内容
化学与生产、生活密切相关,下列说法正确的是( )
| A、小苏打用于治疗胃溃疡病人的胃酸过多症 |
| B、电解从海水中得到的氯化钠溶液可获得金属钠 |
| C、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板 |
| D、铝制容器不能盛放酸性或碱性食品,但可长期盛放腌制食品 |
考点:钠的重要化合物,金属冶炼的一般原理,铝的化学性质,铁盐和亚铁盐的相互转变
专题:几种重要的金属及其化合物
分析:A、小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗;
B、电解食盐水会获得氢氧化钠、氢气和氯气;
C、金属铜可以和三价铁离子反应生成亚铁离子和铜离子.
D、金属铝既能和酸之间反应又能和碱之间反应,在电解质溶液中形成原电池反应,据此回答;
B、电解食盐水会获得氢氧化钠、氢气和氯气;
C、金属铜可以和三价铁离子反应生成亚铁离子和铜离子.
D、金属铝既能和酸之间反应又能和碱之间反应,在电解质溶液中形成原电池反应,据此回答;
解答:
解:A.小苏打与胃酸中的盐酸反应生成氯化钠、水和二氧化碳气体,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,患胃溃疡的病人,为防止胃壁穿孔,不能服用小苏打来治疗,因为反应产生的二氧化碳气体会造成胃部气胀,易造成胃穿孔,故A错误;
B、电解食盐水会获得氢氧化钠、氢气和氯气,电解熔融的氯化钠可以获得金属钠,故B错误;
C、FeCl3溶液能与Cu反应,生成氯化亚铁和氯化铜,可用于蚀刻印刷电路板,故C正确;
D、金属铝既能和酸之间反应又能和碱之间反应,不能盛放酸性或碱性食品,也不能长期盛放腌制食品,里面有氯化钠溶液,会形成原电池而使铝溶解,故D错误.
故选C.
B、电解食盐水会获得氢氧化钠、氢气和氯气,电解熔融的氯化钠可以获得金属钠,故B错误;
C、FeCl3溶液能与Cu反应,生成氯化亚铁和氯化铜,可用于蚀刻印刷电路板,故C正确;
D、金属铝既能和酸之间反应又能和碱之间反应,不能盛放酸性或碱性食品,也不能长期盛放腌制食品,里面有氯化钠溶液,会形成原电池而使铝溶解,故D错误.
故选C.
点评:本题考查了元素以及化合物的性质以及应用是化学的考查热点,注意知识的归纳和整理是关键,较简单.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
在给定条件下,下列加点的物质在化学反应中完全消耗的是( )
A、用50mL8mol?L-1
| ||||||||
B、标准状况下,将1g
| ||||||||
C、向100mL3mol?L-1的稀硝酸中加入5.6g
| ||||||||
D、在5×107Pa、500℃和铁触媒催化的条件下,用
|
物质的量之比为2:5的锌与稀硝酸恰好完全反应,若硝酸被还原的产物为NH4NO3,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
| A、1:4 | B、1:9 |
| C、2:3 | D、2:5 |
下列说法错误的是( )
| A、在水中的溶解度NH3>CH4 |
| B、晶体熔点的高低SiO2>CO2 |
| C、金属键的强弱Li>K |
| D、晶格能的大小NaF>MgO |
下列各组物质中,仅用水及物质间相互反应就能区别的一组是( )
| A、Na2O2、Al2(SO4)3、MgCl2、K2CO3 |
| B、BaCl2、Na2SO4、CaCO3、KOH |
| C、AgNO3、NaCl、KCl、CuCl2 |
| D、Fe2(SO4)3、K2CO3、KHSO4、BaCl2 |
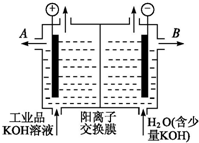 铝和氢氧化钾都是重要的工业产品.请回答:
铝和氢氧化钾都是重要的工业产品.请回答: