题目内容
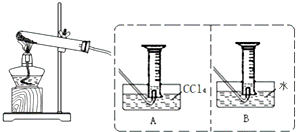
16.常温下,向10mL 0.1mol•L-1的HR溶液中逐滴滴入0.1mol•L-1的NH3•H2O溶液,所得溶液pH及导电性变化如图.下列分析正确的是( )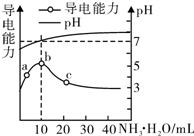
| A. | HR为强酸 | |
| B. | b点溶液呈中性,说明NH4R没有水解 | |
| C. | c点溶液存在c(NH4+)<c( R-) | |
| D. | b~c任意点溶液均有c(H+)×c(OH-)=l.0×l0-14 |
分析 A.根据图知,10mL时混合溶液中酸碱的物质的量相等,二者恰好完全反应生成NH4R,溶液呈中性,且一水合氨是弱碱,则该铵盐是弱酸弱碱盐;
B.b点溶液呈中性,NH4R为弱酸弱碱盐,含有弱离子的盐能水解;
C.c点溶液呈碱性,结合电荷守恒判断铵根离子和酸根离子浓度相对大小;
D.离子积常数只与温度有关,温度不变,则离子积常数不变.
解答 解:A.根据图知,10mL时混合溶液中酸碱的物质的量相等,二者恰好完全反应生成NH4R,溶液呈中性,且一水合氨是弱碱,则该铵盐是弱酸弱碱盐,则HR是弱酸,故A错误;
B.b点溶液呈中性,NH4R为弱酸弱碱盐,含有弱离子的盐能水解,所以该盐能水解,且酸根离子和铵根离子水解程度相等,故B错误;
C.c点溶液呈碱性,则溶液中存在c(H+)<c(OH-),结合电荷守恒得c(NH4+)>c( R-),故C错误;
D.离子积常数只与温度有关,温度不变,则离子积常数不变,所以温度不变b~c任意点溶液均有c(H+)×c(OH-)=l.0×l0-14,故D正确;
故选D.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生图象分析判断能力,正确判断HR酸性强弱是解本题关键,注意C中c点溶液呈碱性而不是酸性,为易错点.

练习册系列答案
相关题目
6.下列关于化学反应速率的说法正确的是( )
| A. | 化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加 | |
| B. | 化学反应速率为“0.8 mol/(L•s)”表示的意思是:时间为1 s时,某物质的浓度为0.8 mol/L | |
| C. | 对于任何化学反应来说,反应速率越大,反应现象越明显 | |
| D. | 根据化学反应速率的大小可以知道化学反应进行的快慢 |
4.重金属盐能使人体中毒,这是由于它使人体内蛋白质( )
| A. | 起盐析作用 | B. | 起变性作用 | C. | 生成尿素 | D. | 水解 |
11.关于乙烯的化学性质,说法错误的是( )
| A. | 可与H2发生加成反应 | B. | 能使溴水褪色 | ||
| C. | 不能发生聚合反应 | D. | 可与酸性高锰酸钾发生氧化反应 |
1.下列实验不能到达到实验目的是( )
| 序号 | 实验操作 | 实验目的 |
| A | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | 向MgCl2、AlCl3溶液中分别通入NH3 | 比较镁、铝金属性强弱 |
| C | 测定相同物质的量浓度的Na2CO3、Na2SO4溶液的pH | 比较碳、硫的非金属性强弱 |
| D | Fe、Cu分别与稀盐酸反应 | 比较铁、铜的金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
8.下列物质中一氯代物有4种的是:( )
| A. | 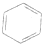 | B. | 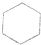 | C. | 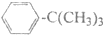 | D. | CH3CH2CH(CH2CH3)2 |
11.一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为55.2g,若其中水的质量为21.6g,则CO的质量为( )
| A. | 2.8g | B. | 4.4g | C. | 8.8g | D. | 4.4~8.8g |