题目内容
14.下列四种物质的结构图中,小黑球代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键,示例:如 ),下列说法正确的是( )
),下列说法正确的是( )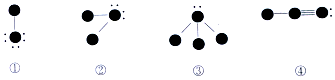
| A. | 四种物质中摩尔质量最大的是③ | B. | ①与③反应生成一种离子化合物 | ||
| C. | ④中含有非极性共价健 | D. | 该四种化合物涉及6种元素 |
分析 根据没有成键的电子数和成键电子数和推知原子的最外层电子数,根据原子序数小于10可知原子的种类,根据结构式可推知化学式;①HF,②H2O;③NH3;④HCN,由此分析解答.
解答 解:A、①HF摩尔质量为:20mol/L,②H2O摩尔质量为:18mol/L;③NH3摩尔质量为:17mol/L;④HCN摩尔质量为:27mol/L,所以摩尔质量最大的是④,故A错误;
B、HF和NH3反应生成离子化合物氟化铵,故B正确;
C、HCN分子中只含极性共价键,故C错误;
D、该四种化合物涉及的元素有H、F、O、N、C五种元素,故D错误;
故选B.
点评 本题考查共价键形成及共价键的主要类型,注意根据形成的共价键数目和孤电子对数判断原子的最外层电子数,以此推断元素的种类,难度中等.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
2. 向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )
向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )
 向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )
向两份完全相同Ba(OH)2溶液中分别加入浓度相同的Al2(SO4)3和KAl(SO4)2,产生的沉淀的物质的量随所加溶液体积关系如图.下列分析不正确的是( )| A. | a、d两点的沉淀为BaSO4 | B. | b、c两点溶液的导电能力相同 | ||
| C. | b、c两点溶液的PH值相同 | D. | d点溶液中大量存在的阳离子是K+ |
9.下列说法正确的是( )
| A. | pH均为2的醋酸和盐酸加水稀释100倍,所得溶液的pH:醋酸>盐酸 | |
| B. | pH为11的氨水和pH为3的盐酸溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol/L的NaOH溶液和CH3COONa溶液等体积混合后的溶液:c(Na+)+c(CH3COO-)=c(OH-)+c(H+) | |
| D. | 浓度均为0.1mol/L的醋酸和CH3COONa溶液等体积混合,溶液中有下列关系:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) |
19.能与氢氧化钠溶液反应的原子晶体且是单质的是( )
| A. | 铝 | B. | 金刚石 | C. | 硅 | D. | 二氧化硅 |
6.已知四苯甲烷的结构式如图,下列有关它的说法中正确的是( )
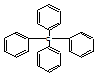

| A. | 它属于苯的同系物 | B. | 分子中所有原子共平面 | ||
| C. | 它的分子式为C25H24 | D. | 它的一氯代物有三种同分异构体 |
4.25℃时,有体积相同的四种溶液:①pH=3的CH3COOH溶液 ②pH=3的盐酸 ③pH=11的氨水 ④pH=11的NaOH溶液.下列说法不正确的是( )
| A. | 若将四种溶液稀释100倍,稀释后溶液pH大小顺序:③>④>②>① | |
| B. | 等体积的③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③>④ | |
| C. | 等体积的②和③混合生成强酸弱碱盐,混合后溶液呈酸性 | |
| D. | 等体积的①和②分别与足量的锌粒反应生成的氢气在同温同压下体积:①>② |
