题目内容
18.A-J是中学化学常见的物质,它们之间的转化关系如图所示(部分产物已略去).已知A 是一种高熔点物质,D 是一种红棕色固体.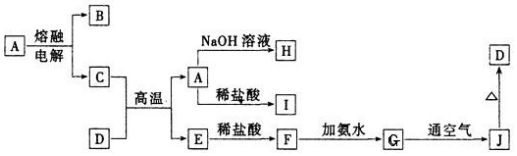
请回答下列问题:
(1)D 物质的俗名为赤铁矿,H 与 I 反应离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓.
(2)C 与 D 在高温下的反应在冶金工业上称为铝热反应,写出该反应化学方程式并用单线桥表示电子
转移
(3)写出 F→G、G→J 的化学方程式:FeCl2+2NH3•H2O=Fe(OH)2↓+2NH4Cl、4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(4)A→H 的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
分析 D是一种红棕色固体可知D为Fe2O3,A是一种高熔点物质,电解A得到B与C,考虑A为Al2O3,由转化关系C+Fe2O3$\stackrel{高温}{→}$A(Al2O3)+E,故C为Al,E为Fe,A能与氢氧化钠溶液、盐酸反应,A为Al2O3符合转化关系,故B为O2;A与氢氧化钠溶液生成H,A与盐酸反应生成I,故H为NaAlO2,I为AlCl3,E(Fe)与盐酸反应生成F,故F为FeCl2,F(FeCl2溶液)中加入氨水生成G,G$\stackrel{O_{2}}{→}$J$\stackrel{△}{→}$D(Fe2O3),故G为Fe(OH)2,J为Fe(OH)3,验证符合转化关系,结合对应物质的性质以及题目要求解答该题.
解答 解:(1)D是一种红棕色固体可知D为Fe2O3,俗名为赤铁矿,H为NaAlO2,I为AlCl3,NaAlO2和AlCl3互相促进水解,离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:赤铁矿;Al3++3AlO2-+6H2O=4Al(OH)3↓;
(2)C与D在高温下的反应为2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,在反应中,Al元素化合价升高值=Fe元素合价降低值=转移电子数=6,用单线桥表示反应中的电子转移情况如下: ,故答案为:
,故答案为: ;
;
(3)F→G是FeCl2溶液中加入氨水生成Fe(OH)2,反应方程式为:FeCl2+2NH3•H2O=Fe(OH)2↓+2NH4Cl,
G→J是Fe(OH)2被氧化为Fe(OH)3,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:FeCl2+2NH3•H2O=Fe(OH)2↓+2NH4Cl;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(4)A→H是氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应离子方程式为:Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O.
点评 本题是一道典型的无机框图推断题,为高考常见题型,侧重于考查对元素化合物基础知识的掌握,还主要考查学科内知识间的综合推理能力,难度中等,突破口为:D物质的颜色,A的分解条件及A能与氢氧化钠溶液、盐酸反应,利用猜测验证法推断,题目难度中等.

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案| A. | 含20.0gNaOH的稀溶液与足量稀硫酸完全中和,放出28.7kJ的热量,则表示中和热的热化学方程式为2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(1)△H=-114.8kJ/mol | |
| B. | 已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为196.64kJ | |
| C. | 已知2H2(g)+O2(g)═2H2O(g);△H=-483.6kJ/mol,则H2的燃烧热为241.8kJ/mol | |
| D. | 已知H+(aq)+OH-(aq)═H2O(1)△H=-57.31kJ•mol-1,故Ba2+(aq)+H+(aq)+OH-(aq)+SO42-(aq)═H2O(1)+BaSO4(s)△H<-57.31kJ•mol-1 |
| A. | pH均为2的醋酸和盐酸加水稀释100倍,所得溶液的pH:醋酸>盐酸 | |
| B. | pH为11的氨水和pH为3的盐酸溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol/L的NaOH溶液和CH3COONa溶液等体积混合后的溶液:c(Na+)+c(CH3COO-)=c(OH-)+c(H+) | |
| D. | 浓度均为0.1mol/L的醋酸和CH3COONa溶液等体积混合,溶液中有下列关系:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) |
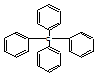
| A. | 它属于苯的同系物 | B. | 分子中所有原子共平面 | ||
| C. | 它的分子式为C25H24 | D. | 它的一氯代物有三种同分异构体 |
| A. | 金属铯的密度比金属钠小 | B. | 金属铯的熔点比金属钠高 | ||
| C. | Cs与H2O能剧烈反应,甚至发生爆炸 | D. | 碳酸铯难溶于水 |
| A. | 8 | B. | 9 | C. | 11 | D. | 12 |