题目内容
11.在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
| A. | 碳棒上有气体放出,溶液pH变小 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,外电路中,电流从a极到b极 | |
| D. | a极上发生了氧化反应 |
分析 金属a能从酸中置换出H2,b为碳棒,则a属于氢之前的金属,该装置构成原电池,a为负极、b为正极,电流则从正极沿导线流向负极,据此分析解答.
解答 解:金属a能从酸中置换出H2,b为碳棒,则a属于氢之前的金属,该装置构成原电池,a为负极、b为正极,
A.碳棒上氢离子得电子生成氢气,溶液中氢离子浓度减小,溶液的PH增大,故A错误;
B.通过以上分析知,a是负极、b是正极,故B错误;
C.该装置构成原电池,导线中有电子流动,外电路中,电流则从正极极b沿导线流向负极a,故C错误;
D.a电极上金属失电子发生氧化反应,故D正确;
故选D.
点评 本题考查了原电池原理,明确正负极的判断、电子流向、电极上的反应等知识点即可解答,难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
16.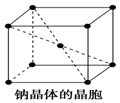 金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
 金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶格(如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(molC-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )| A. | $\root{3}{\frac{2a}{{N}_{A}ρ}}$ | B. | $\sqrt{2}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ | C. | $\frac{\sqrt{3}}{4}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ | D. | $\frac{1}{2}$$\root{3}{\frac{2a}{{N}_{A}ρ}}$ |
14.下列有关苯、乙酸、乙醇说法正确的是( )
| A. | 都易溶于水 | |
| B. | 苯易挥发不能用作溶剂 | |
| C. | 乙醇和乙酸反应的有机产物的同分异构体中属于酯类的有4种 | |
| D. | CH3CH2OH→CH3CHO发生了加成反应 |
6.在复杂的体系中,研究化学反应的先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是( )
| A. | 含有等物质的量的AlO2-,OH-,CO32-的溶液中逐滴加入盐酸:AlO2-,OH-,CO32- | |
| B. | 含有等物质的量的FeBr2和FeI2溶液中缓缓通入Cl2:I-,Br-,Fe2+ | |
| C. | 在等物质的量的Ba(OH)2和KOH溶液中缓缓通入CO2:KOH,Ba(OH)2,BaCO3 | |
| D. | 在含有等物质的量的Fe3+、Ag+、Cu2+、H+、Fe2+的溶液中逐渐加入锌粉:Ag+、Fe3+、Cu2+、H+、Fe2+ |
16.自来水中因含有少量Cl-而不能用于溶液的配制,实验室为了除去自来水中的Cl-获得纯净水,可采用的方法是( )
| A. | 过滤法 | B. | 结晶法 | C. | 蒸馏法 | D. | 沉淀法 |
3.分类是科学研究的重要依据,下列物质分类不正确的是( )
| A. | 混合物:铝热剂、液氨、铝合金、酒精 | |
| B. | 化合物:干冰、冰水混合物、烧碱、小苏打 | |
| C. | 电解质:氯化钠、硫酸钡、氯化氢、水 | |
| D. | 同素异形体:活性炭、C60、石墨烯、金刚石 |
20.下列电离方程式错误的是( )
| A. | NaHCO3=Na++H++CO32- | B. | NaHSO4=Na++H++SO42- | ||
| C. | H2SO4=2H++SO42- | D. | CH3COOH?CH3COO-+H+ |
1.下列除杂的方法中,正确的是( )
| A. | 除去淀粉溶液中的NaCl:加入AgNO3溶液后,静置过滤 | |
| B. | 除去乙烷中少量的乙烯:光照下通入Cl2,生成液态CH2Cl-CH2Cl,气液分离 | |
| C. | 除去CO2中少量的乙烯:通过酸性KMnO4溶液 | |
| D. | 除去乙酸乙酯中的乙酸:用NaOH溶液中和,然后蒸馏 |
