题目内容
18.下列叙述正确的是( )| A. | 食盐水克导电,所以食盐水是电解质 | |
| B. | NH3的水溶液能够导电,所以NH3电解质 | |
| C. | 蔗糖溶于水不导电,所以蔗糖是非电解质 | |
| D. | BaSO4投入水中,导电性极弱,所以BaSO4是弱电解质 |
分析 水溶液中或熔融状态下导电的化合物为电解质,水溶液中和熔融状态下都不导电的化合物为非电解质,水溶液中部分电离的电解质为弱电解质,水溶液中完全电离的电解质为强电解质,据此分析判断.
解答 解:A.食盐水为氯化钠的水溶液属于混合物,属于电解质溶液,故A错误;
B.NH3的水溶液能够导电,但氨气不能电离所以NH3 是非电解质,故B错误;
C.蔗糖溶于水不导电,熔融状态也不导电,所以蔗糖是非电解质,故C正确;
D.BaSO4投入水中,导电性极弱,熔融状态下完全电离能导电,所以BaSO4是强电解质,故D错误;
故选C.
点评 本题考查了电解质、非电解质、强电解质、弱电解质概念的分析判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
6.下列离子方程式的书写正确的是( )
| A. | 实验室用大理石和稀盐酸制取CO2:CO32-+2H+═CO2↑+H2O | |
| B. | Al(OH)3加入NaOH溶液:Al(OH)3+OH-═AlO2-+2H2O | |
| C. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | 向偏铝酸钠溶液通入过量的CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
3.NA为阿伏加德罗常数的值,下列说法错误的是( )
| A. | 10.0 g CaCO3与足量稀盐酸反应,消耗H+的数目为0.2 NA | |
| B. | 0.1 mol Ar所含的原子数为0.1NA | |
| C. | 200 mL 0.1 mol/L的Na2SO4中含Na+数目为0.04NA | |
| D. | 25℃、101 kPa时,Zn与稀硫酸反应生成2.24 L H2,转移的电子总数为0.2NA |
10.天然皮革是( )
| A. | 纤维素制品 | B. | 脂肪类物质 | ||
| C. | 橡胶制品 | D. | 凝固和变性的蛋白质 |
7.向烧杯中加入一定量的蔗糖,加水湿润后,加入浓硫酸搅拌,经过一系列的变化以后形成“黑面包”.在此实验中不能体现出浓硫酸的性质是( )
| A. | 吸水性 | B. | 脱水性 | C. | 强氧化性 | D. | 酸性 |
8.下列各组物质、按单质、电解质、混合物顺序排列的是( )
| A. | 铁、纯碱、冰水混合物 | B. | 氢气、陶瓷、漂白粉 | ||
| C. | 液氧、烧碱、碘酒 | D. | 金刚石、二氧化碳、漂粉精 |
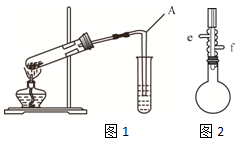 酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,表格中给出了一些物质的物理常数,请回答下列问题
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业,表格中给出了一些物质的物理常数,请回答下列问题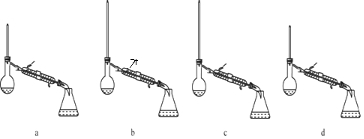
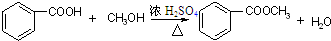 .
.