题目内容
10.某液体化合物X2Y4常用做火箭燃料,16gX2Y4在一定量的O2中恰好完全燃烧:X2Y4 (l)+O2(g)$\frac{\underline{\;点燃\;}}{\;}$X2(g)+2Y2O(l).冷却后测得生成物体积为11.2L(标准状况下,下同),密度为1.25g•L-1,则:(1)反应前O2的体积为11.2L;X2Y4做火箭燃料的理由(只答一点)是反应生成的产物无污染.
(2)X2的摩尔质量为28g/mol;Y元素的名称是氢.
(3)X2Y4中X元素的化合价为-2;若反应生成0.1molX2,则转移0.4mol电子.
分析 (1)由方程式可知,反应前后气体的体积不发生变化,据此计算氧气的体积;反应生成的产物无污染;
(2)标准状况下,气体摩尔质量M=Vm×ρ,据此计算气体X2的摩尔质量;根据方程式计算的物质的量X2Y4,再计算X2Y4的相对分子质量,进而计算Y的相对原子质量,确定Y元素名称;
(3)根据化合价的变化计算.
解答 解:标准状况下,气体X2的摩尔质量=22.4L/mol×1.25g/L=28g/mol,
11.2L X2的物质的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,Mr(X2Y4)=$\frac{16}{0.5}$=32,Y的相对原子质量=$\frac{32-28}{4}$=1,故Y为氢元素,可知X2Y4为N2H4,
(1)由方程式可知,反应前后气体的体积不发生变化,X2和氧气的关系式为1:1,故V(O2)=V(X2)=11.2L,反应生成氮气和水,反应生成的产物无污染;
故答案为:11.2L;反应生成的产物无污染;
(2)标准状况下,气体摩尔质量M=Vm×ρ,气体X2的摩尔质量=22.4L/mol×1.25g/L=28g/mol,
11.2L X2的物质的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,n(X2Y4)=n(X2)=0.5mol,故Mr(X2Y4)=$\frac{16}{0.5}$=32,则Y的相对原子质量=$\frac{32-28}{4}$=1,故Y为氢元素,
故答案为:28g/mol;氢;
(3)X2Y4的化学式为X2H4,H为+1价,则X的化合价为-2价,反应中X化合价由-2价升高到0价,由方程式可知,生成1molX2,则转移4mol电子,若反应生成0.1mol X2,则转移电子的物质的量为0.4mol.
故答案为:-2;0.4.
点评 本题考查化学方程式的有关计算,难度不大,注意根据方程式的特征计算氧气的体积,理解气体的摩尔质量与密度的关系.

| A. | 在标准状况下,NA个CHCl3分子所占的体积约为22.4L | |
| B. | 苯分子中的所有原子都在同一个平面上 | |
| C. | 点燃甲烷必须事先进行验纯 | |
| D. | 甲烷燃烧能放出大量的热,所以是一种很好的气体燃料 |

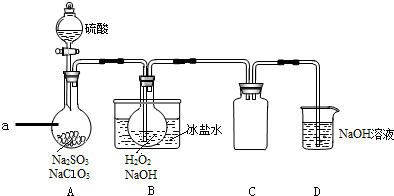
| A. | 图4为用浓硝酸溶液与铜反应制备并收集少量NO2 | |
| B. | 图2为制备少量氧气 | |
| C. | 图3为配制一定物质的量浓度的硫酸溶液 | |
| D. | 图1为证明非金属性强弱:S>C>Si |
| A. | HNO3具有氧化性 | B. | NH3既具有氧化性又具有还原性 | ||
| C. | N2只具有还原性 | D. | NO2既具有氧化性又具有还原性 |
 如图(Ⅰ)表示反应:mA(g)+nB(g)?pC(g)+qD(g);△H.在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系.图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变压强,重新建立平衡的反应过程.由此可判断该反应中( )
如图(Ⅰ)表示反应:mA(g)+nB(g)?pC(g)+qD(g);△H.在不同温度下经过一定时间混合气体体系中C的百分含量与温度T的关系.图(Ⅱ)表示在一定条件下达到平衡后,t时刻改变压强,重新建立平衡的反应过程.由此可判断该反应中( )| A. | m+n>p+q,△H<0 | B. | m+n>p+q,△H>0 | C. | m+n<p+q,△H>0 | D. | m+n<p+q,△H<0 |
| A. | 生成0.3 mol Cl2时,转移电子的物质的量为0.6 mol | |
| B. | 该反应中,生成的Cl2的摩尔质量约为70.7 g/mol | |
| C. | 被0.1 mol K37ClO3氧化的H35Cl的物质的量为0.6 mol | |
| D. | 该反应中,H35Cl发生氧化反应,KCl是还原产物 |
| A. | SO2、O2、H2S | B. | H2、O2、F2 | C. | O2、C12、HBr | D. | H2S、CO2、H2 |
| A. |  含0.01molKOH 和0.01mol Ca(OH)2 的混合溶液中缓慢通入CO2 | |
| B. |  n(O2)=1mol时,高温下C和O2在密闭容器中的反应产物 | |
| C. |  KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液 | |
| D. |  n(NaOH)=1mol时,CO2和NaOH溶液反应生成的盐 |