题目内容
20.下列示意图与对应的反应情况正确的是( )| A. |  含0.01molKOH 和0.01mol Ca(OH)2 的混合溶液中缓慢通入CO2 | |
| B. | 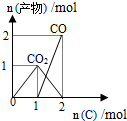 n(O2)=1mol时,高温下C和O2在密闭容器中的反应产物 | |
| C. | 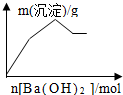 KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液 | |
| D. | 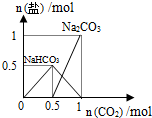 n(NaOH)=1mol时,CO2和NaOH溶液反应生成的盐 |
分析 A.发生的反应为:Ca(OH)2+CO2=CaCO3↓+H2O、2KOH+CO2=K2CO3+H2O、CaCO3+CO2+H2O=Ca(HCO3)2、K2CO3+CO2+H2O=2KHCO3,当KOH完全反应后,碳酸钙再和二氧化碳反应;
B.C.当n(C)≤1mol时,发生的反应为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,当n(C)>1mol时,发生的反应为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
C.向硫酸铝钾中滴入氢氧化钠溶液时发生的离子方程式有Ba2++SO42-═BaSO4↓、Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,根据物质间的反应判断;
D.当0<n(CO2)≤0.5mol时,发生的反应为2NaOH+CO2=Na2CO3+H2O,当0.5mol<n(CO2)≤1mol,发生的反应为NaOH+CO2=NaHCO3.
解答 解:A.发生的反应为:Ca(OH)2+CO2=CaCO3↓+H2O、2KOH+CO2=K2CO3+H2O、CaCO3+CO2+H2O=Ca(HCO3)2、K2CO3+CO2+H2O=2KHCO3,当KOH完全反应后,碳酸钙再和二氧化碳反应,生成碳酸钙、消失碳酸钙、和氢氧化钾反应生成碳酸钾需要二氧化碳的物质的量之比为2:2:1,所以其图象应该是 ,故A错误;
,故A错误;
B.C.当n(C)≤1mol时,发生的反应为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,当n(C)>1mol时,发生的反应为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,所以其图象为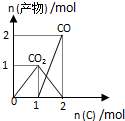 ,故B正确;
,故B正确;
C.向硫酸铝钾中滴入氢氧化钠溶液时发生的离子方程式有Ba2++SO42-═BaSO4↓、Al3++3OH-═Al(OH)3↓、Al(OH)3+OH-═AlO2-+2H2O,假设n(KAl(SO4)2)=2mol,当n(Ba(OH)2)≤3mol,发生的反应为Ba2++SO42-═BaSO4↓、Al3++3OH-═Al(OH)3↓,沉淀的质量为m(BaSO4)+m(Al(OH)3),铝离子完全沉淀时,还剩n(SO42-)=1mol;
当3mol<n(Ba(OH)2)≤4mol,发生的反应为Ba2++SO42-═BaSO4、Al(OH)3+OH-═AlO2-+2H2O,沉淀的质量为硫酸钡减去溶解的氢氧化铝的质量,硫酸根离子完全沉淀时,铝元素完全转化为偏铝酸根离子,生成的n(BaSO4),溶解的n(Al(OH)3)=2mol,固体增加质量=233g/mol×1mol-78g/mol×2mol=77g>0,再继续加入氢氧化钡溶液,固体的质量不变,所以其图象为 ,故C错误;
,故C错误;
D.当0<n(CO2)≤0.5mol时,发生的反应为2NaOH+CO2=Na2CO3+H2O,当0.5mol<n(CO2)≤1mol,发生的反应为NaOH+CO2=NaHCO3,所以其图象为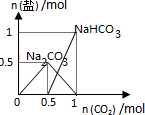 ,故D错误;
,故D错误;
故选B.
点评 本题考查了化学反应与化学图象的判断,题目难度中等,明确物质间的反应及物质的性质是解本题关键,根据物质之间量的关系进行解答,难点是根据其分界点确定发生的反应.

| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
 如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )
如图所示装置,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )| A. | 2:7 | B. | 5:4 | C. | 4:5 | D. | 7:3 |
| A. | 用中和法除去废水中的酸 | B. | 用混凝剂除去废水中的重金属离子 | ||
| C. | 用氯气除去废水中的悬浮物 | D. | 用臭氧除去废水中的异味 |
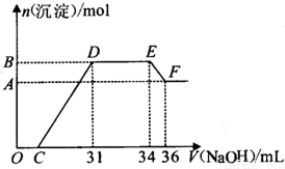
| A. | OC段离子反应方程式为H++OH-═H2O | |
| B. | 溶液中n(NH${\;}_{4}^{+}$)=0.012 mol | |
| C. | 溶液中结合OH-能力最强的离子是H+,最弱的离子是Al3+ | |
| D. | 欲测定F点沉淀的质量,实验步骤是:过滤、洗涤、干燥、称量 |
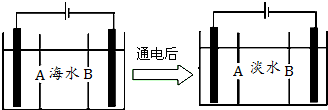
 ;
;