题目内容
13.Cu2O是一种半导体材料,基于绿色化学理念设计的一制取Cu2O的电解池示意图如下,电池总反应为2Cu+H2O$\frac{\underline{\;电解\;}}{\;}$Cu2O+H2↑.下列说法正确的是( )
| A. | 石墨电极上产生氢气 | |
| B. | 铜电极被还原 | |
| C. | 铜电极接直流电源的负极 | |
| D. | 当有1 mol电子转移时,有1 mol Cu2O生成 |
分析 根据电解总反应为2Cu+H2O═Cu2O+H2↑可以知道金属为阳极材料,在阳极发生失电子的氧化反应,在阴极上是氢离子发生得电子的还原反应,据此分析.
解答 解:A、电解总反应:2Cu+H2O═Cu2O+H2↑,金属铜失电子,说明金属铜一定作阳极,石墨做阴极,在阴极上是溶液中的氢离子得电子,产生氢气,故A正确;
B、铜电极本身失电子,发生氧化反应,故B错误;
C、铜电极是电解池的阳极,与直流电源的正极相连,故C错误;
D、反应2Cu+H2O═Cu2O+H2↑失电子物质的量为2mol,生成氧化亚铜1mol,所以当有1mol电子转移时,有0.5molCu2O生成,故D错误.
故选A.
点评 本题考查学生电解池的工作原理,注意根据电解池的总反应来判断阴阳极以及两极上发生的反应,题目难度不大.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案
相关题目
1.下列说法中正确的是( )
| A. | HF、HCl、HBr、HI的热稳定性依次减弱,沸点依次升高 | |
| B. | NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏离子键和共价键 | |
| C. | 熔融状态下能导电的化合物一定含离子键 | |
| D. | CS2、BF3分子中所有的原子均为8电子稳定结构 |
8.某化合物的结构(键线式)及球棍模型如下:

该有机分子的核磁共振波谱图如下(单位是ppm).
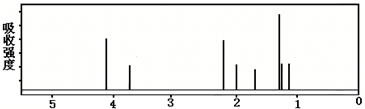
下列关于该有机物的叙述正确的是( )

该有机分子的核磁共振波谱图如下(单位是ppm).

下列关于该有机物的叙述正确的是( )
| A. | 键线式中的Et代表的基团为-CH3 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 该有机物不同化学环境的氢原子有8种 | |
| D. | 该有机物不可能发生消去反应 |
18.常温下,1mol某烷烃在光照条件下与氯气发生取代反应,若在适当的条件下,完全取代需要消耗6mol Cl2,则下列判断正确的是( )
| A. | 该烷烃的分子式为C5H12 | |
| B. | 反应所生成的有机产物能直接使AgNO3溶液褪色 | |
| C. | 该烷烃的四氯代物有2种 | |
| D. | 反应容器中,一氯代物所占的物质的量分数最大 |
5.下列说法错误的是( )
| A. | 除氦外的稀有气体原子的最外层电子数都是8 | |
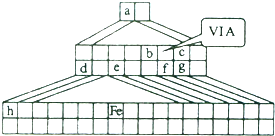
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| D. | 同一元素的各种同位素的化学性质均相同 |
2.下列说法错误的是( )
| A. | 酒精可以和水以任意比例互溶,与氢键有关 | |
| B. | 邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点,与氢键有关 | |
| C. | 无机含氧酸的化学式可以用XOn(OH)m表示,n值越大,m值越小,则该酸的酸性就越强.则可推知,硫酸酸性强于磷酸 | |
| D. | 两分子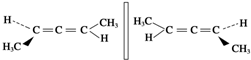 互为手性分子 互为手性分子 |
3.下列有关实验原理或实验操作正确的是( )
| A. | 用NaOH溶液滴定CH3COOH溶液,可选用甲基橙作指示剂 | |
| B. | 用量筒量20mL0.5000mol•L-1H2SO4溶液于烧杯中,加水80mL,配制成0.1000mol•L-1H2SO4溶液 | |
| C. | 常温下,物质的量浓度均为0.1mol•L-1的盐酸、醋酸溶液,分别用水稀释100倍后pH的关系为:盐酸>醋酸 | |
| D. | 实验室常将氯化铁先溶于盐酸,再加水稀释来配制其溶液 |
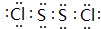 ;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的化学方程式:2S2Cl2+2H2O=3S+SO2↑+4HCl;
;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的化学方程式:2S2Cl2+2H2O=3S+SO2↑+4HCl;